Радон — это… Что такое Радон?
| Внешний вид простого вещества | |
|---|---|
Бесцветный, слегка флюоресцирующий радиоактивный газ | |
| Свойства атома | |
| Имя, символ, номер | Радо́н / Radon (Rn), 86 |
| Атомная масса (молярная масса) | 222,0176 а. е. м. (г/моль) |
| Электронная конфигурация | [Xe] 4f14 5d10 6s2 6p6 |
| Радиус атома | 214 пм |
| Химические свойства | |
| Ковалентный радиус | 140—150 пм |
| Степени окисления | 0 |
| Энергия ионизации (первый электрон) | 1036,5(10,74) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | (газ, при 0 °C) 9,81 кг/м3 |
| Температура плавления | 202 (-71,15 °C) |
| Температура кипения | 211,4 (-61,75 °C) |
| Теплота плавления | 2,7 кДж/моль |
| Теплота испарения | 18,1 кДж/моль |
| Молярная теплоёмкость | 20,79[1] Дж/(K·моль) |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая |
| Прочие характеристики | |
| Теплопроводность | (300 K) (газ, при 0 °C) 0,0036 Вт/(м·К) |
| 86 | Радон |
| 4f145d106s2 6p6 | |
Радо́н — элемент главной подгруппы восьмой группы, шестого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 86. Обозначается символом Rn (Radon). Простое вещество радон (CAS-номер: 10043-92-2) при нормальных условиях — бесцветный инертный газ; радиоактивен, может представлять опасность для здоровья и жизни. При комнатной температуре является одним из самых тяжелых газов. Наиболее стабильный изотоп (222Rn) имеет период полураспада 3,8 суток.
История открытия и происхождение названия
Английский учёный Э. Резерфорд в 1899 году отметил, что препараты тория испускают, кроме α-частиц, и некое неизвестное ранее вещество, так что воздух вокруг препаратов тория постепенно становится радиоактивным. Это вещество он предложил назвать эмана́цией (от латинского emanatio — истечение) тория и дать ему символ Em. Последующие наблюдения показали, что и препараты радия также испускают некую эманацию, которая обладает радиоактивными свойствами и ведет себя как инертный газ.
Первоначально эманацию тория называли торо́ном, а эманацию радия — радо́ном. Было доказано, что все эманации на самом деле представляют собой радионуклиды нового элемента — инертного газа, которому отвечает атомный номер 86. Впервые его выделили в чистом виде Рамзай и Грей в 1908 году, они же предложили назвать газ нитон (от лат. nitens, светящийся). В 1923 году газ получил окончательное название радон и символ Em был сменён на Rn.
В публичной лекции 1936 г. Резерфорд кратко изложил итоги их работ:
Я помогал ему [профессору по электротехнике Оуэнсу в университете МакГилл в г. Монреале в Канаде с декабря 1898 г. по 26 мая 1899 г.] в проведении экспериментов, и мы обнаружили некоторые очень странные явления. Оказалось, что радиоактивное воздействие окиси тория может проходить сквозь дюжину листков бумаги, положенных поверх этой окиси, но задерживается тончайшей пластинкой слюды, как будто излучается что-то, способное диффундировать сквозь поры бумаги. Тот факт, что прибор был очень чувствителен к движению воздуха, поддерживал эту диффузионную гипотезу. Затем мы провели эксперименты, в которых воздух проходил над окисью тория, а потом попадал в ионизационную камеру. Эти опыты показали, что активность может переноситься воздухом. Однако, когда поток воздуха прекращался, активность в ионизационной камере не сразу исчезала, а уменьшалась постепенно по экспоненциальному закону. Я назвал это газообразное вещество, которое может диффундировать сквозь бумагу, переноситься воздухом и в течение некоторого времени сохранять свою активность, исчезающую по характерному закону, «эманацией тория». Я установил, что эта эманация обладает чрезвычайно своеобразным свойством делать радиоактивными тела, над которыми она проходит. Казалось, что это свойство, скорее всего, обусловлено осаждением некой материальной субстанции, а не какой-либо активностью, возникшей в самих телах под действием излучения, так как тогда количество осажденного вещества должно увеличиваться при приложении электрического поля. В те времена многие получали неповторяющиеся и странные результаты, помещая предметы вблизи радиоактивных веществ. По-видимому, все это могло объясняться наличием таких же эманаций, как обнаруженная нами у тория. Прежде чем считать такое объяснение правильным, необходимо было выяснить истинную природу эманации. Это было очень трудно, так как доступное количество ее всегда было очень мало.
Заслуга открытия радона, как химического элемента, часто приписывается также немецкому химику Фредерику Эрнсту Дорну (en:Friedrich Ernst Dorn, 1848—1916). Вопросы приоритета в открытии радона рассматриваются в работе Джеймса и Вирджинии Маршалл[2], где показано, что первооткрывателем радона как химического элемента следует считать Резерфорда. В 1900 г. Дорн открыл изотоп радона-222 с периодом полураспада 3,823 дня и опубликовал статью об этом, сославшись на более раннюю работу Резерфорда. Резерфорд, сперва с Оуэнсом, а затем один в 1899 г. работал с другим изотопом Rn-220 (тороном), период полураспада которого около 54,5 секунд. Резерфорд не знал о работах немца, так как тот опубликовал свою работу в немецком журнале с небольшим тиражом. Резерфорд не знал немецкого. Дорн совершенно не интересовался радиоактивностью. И только в 1902 г. Резерфорд и Содди экспериментально доказали, что эманация — это изотоп радона. Они сумели её охладить и превратить в жидкость с помощью новой физической установки в университете МакГилл и опубликовали статьи.
Нахождение в природе
Входит в состав радиоактивных рядов 238U, 235U и 232Th. Ядра радона постоянно возникают в природе при радиоактивном распаде материнских ядер. Равновесное содержание в земной коре 7·10−16% по массе. Ввиду химической инертности радон относительно легко покидает кристаллическую решётку «родительского» минерала и попадает в подземные воды, природные газы и воздух. Поскольку наиболее долгоживущим из четырёх природных изотопов радона является
Концентрация радона в воздухе зависит, в первую очередь, от геологической обстановки (так, граниты, в которых много урана, являются активными источниками радона, в то же время над поверхностью морей радона мало), а также от погоды (во время дождя микротрещины, по которым радон поступает из почвы, заполняются водой; снежный покров также препятствует доступу радона в воздух). Перед землетрясениями наблюдалось повышение концентрации радона в воздухе, вероятно, благодаря более активному обмену воздуха в грунте ввиду роста микросейсмической активности.
Получение
Для получения радона через водный раствор любой соли радия продувают воздух, который уносит с собой образующийся при радиоактивном распаде радия радон. Далее воздух тщательно фильтруют для отделения микрокапель раствора, содержащего соль радия, которые могут быть захвачены током воздуха. Для получения собственно радона из смеси газов удаляют химически активные вещества (кислород, водород, водяные пары и т. д.), остаток конденсируют жидким азотом, затем из конденсата отгоняют азот и инертные газы (аргон, неон и т.д).
Физические свойства
Радон — радиоактивный одноатомный газ без цвета и запаха. Растворимость в воде 460 мл/л; в органических растворителях, в жировой ткани человека растворимость радона в десятки раз выше, чем в воде. Газ хорошо просачивается сквозь полимерные плёнки. Легко адсорбируется активированным углем и силикагелем.
Собственная радиоактивность радона вызывает его флюоресценцию. Газообразный и жидкий радон флюоресцирует голубым светом, у твёрдого радона при охлаждении до азотных температур цвет флюоресценции становится сперва жёлтым, затем красно-оранжевым.
Цвет свечения в газовом разряде у радона — синий, так как в видимой части спектра радона особо выделяются 8 линий, отвечающих длинам волн от 3982 до 5085 Å и лежащих главным образом в синей части спектра
Химические свойства
«Благородный газ». Однако радон является наиболее активным благородным газом в химическом отношении, так как его валентные электроны находятся на максимальном удалении от ядра. Радон образует клатраты, которые, хотя и имеют постоянный состав, химических связей с участием атомов радона в них нет. С фтором радон при высоких температурах образует соединения состава RnFn, где n = 4, 6, 2. Так, дифторид радона RnF2 является белым нелетучим кристаллическим веществом. Фториды радона могут быть получены также под действием фторирующих агентов (например, фторидов галогенов). При гидролизе тетрафторида RnF4 и гексафторида RnF6 образуется оксид радона RnO3. Получены также соединения с катионом RnF+.
Применение
Радон используют в медицине для приготовления радоновых ванн. Радон используется в сельском хозяйстве для активации кормов домашних животных [1], в металлургии в качестве индикатора при определении скорости газовых потоков в доменных печах, газопроводах. В геологии измерение содержания радона в воздухе и воде применяется для поиска месторождений урана и тория, в гидрологии — для исследования взаимодействия грунтовых и речных вод. Динамика концентрации радона в подземных водах может применяться для прогноза землетрясений[4].
История вопроса
Открытие радиоактивности и радона совпало с повышением интереса к биологическим эффектам радиации. Было установлено, что вода многих источников минеральных вод богата эманацией радия (так именовался радон в то время). Вслед за этим открытием последовала волна моды «на радиацию». В частности, в рекламе того времени радиоактивность минеральных вод выдавалась за главный показатель их полезности и эффективности.
Естественный радиационный фон помещений зданий
Основные составляющие радиационного фона помещений в значительной степени зависят от деятельности человека. Это вызвано, прежде всего, такими факторами, как выбор строительных материалов, конструктивных решений зданий и применяемых в них систем вентиляции
Биологическое воздействие
Попадая в организм человека, радон способствует процессам, приводящим к раку лёгких. Распад ядер радона и его дочерних изотопов в легочной ткани вызывает микроожог, поскольку вся энергия альфа-частиц поглощается практически в точке распада. Особенно опасно (повышает риск заболевания) сочетание воздействия радона и курения. Считается, что радон — второй по частоте (после курения) фактор, вызывающий рак лёгких преимущественно бронхогенного (центрального) типа. Рак лёгких, вызванный радоновым облучением, является шестой по частоте причиной смерти от рака[6].
Радионуклиды радона обусловливают более половины всей дозы радиации, которую в среднем получает организм человека от природных и техногенных радионуклидов окружающей среды.
В настоящее время во многих странах проводят экологический мониторинг концентрации радона в зданиях, так как в районах геологических разломов его концентрации в помещениях зданий могут носить ураганный характер и существенно превышать средние значения по остальным регионам.
Предельно допустимое поступление радона-222 через органы дыхания равно 146 МБк/год[1].
Изотопы
Радон не имеет стабильных изотопов. Наиболее устойчив 222Rn (T1/2=3,8235 дня), входящий в природное радиоактивное семейство урана-238 (семейство урана-радия) и являющийся непосредственным продуктом распада радия-226. Иногда название «радон» относят именно к этому изотопу. В семейство тория-232 входит 220Rn (T1/2=55,6 с), иногда его называют торон (Tn). В семейство урана-235 (урана-актиния) входит 219Rn (T1/2=3,96 с), его называют актинон (An). В одну из побочных ветвей (коэффициент ветвления 2·10−7) семейства урана-радия входит также очень короткоживущий (T1/2=35 мс) радон-218. Все отмеченные изотопы радона испытывают альфа-распад. Этими четырьмя нуклидами исчерпывается список природных изотопов радона. Известны ещё 30 искусственных изотопов Rn с массовым числом от 195 до 228. Некоторые нейтронодефицитные изотопы радона имеют также возбуждённые метастабильные состояния; таких состояний известно 13. Преобладающие моды распада у лёгких изотопов Rn — альфа-распад, позитронный распад и электронный захват. Начиная с массового числа A=212 альфа-распад становится доминирующим. Тяжёлые изотопы радона (начиная с A=223) распадаются преимущественно посредством бета-минус-распада.
Примечания
- ↑ 1 2 3 Редкол.:Зефиров Н. С. (гл. ред.) Химическая энциклопедия: в 5 т. — Москва: Советская энциклопедия, 1995. — Т. 4. — С. 174. — 639 с. — 20 000 экз. — ISBN 5—85270—039—8
- ↑ James L. Marshall and Virginia R. Marshall (2003). «ERNEST RUTHERFORD, THE «TRUE DISCOVERER» OF RADON». Bulletin for the History of Chemistry 28 (2): 76-83.
- ↑ Библиотека НЕФТЬ-ГАЗ
- ↑ Уткин В. И., Юрков А. К. Динамика выделения радона из массива горных пород как краткосрочный предвестник землетрясения // Докл. РАН. 1998. Т.358. № 5. С.675-680.
- ↑ Назиров, Р. А. Снижение естественной радиоактивности цементных бетонов / Р. А. Назиров, Е. В. Пересыпкин, И. В. Тарасов, В. И. Верещагин // Научно-теоретический журнал Известия вузов «Строительство» — Новосибирск: НГАСУ, 2007. С. 45-49.
- ↑ S. Darby, D. Hill, R. Doll (2001). «Radon: A likely carcinogen at all exposures». Annals of Oncology 12 (10): 27. DOI:10.1023/A:1012518223463.
Ссылки
Радон — Википедия
| Внешний вид простого вещества | |
|---|---|
Бесцветный, слегка флюоресцирующий радиоактивный газ | |
| Свойства атома | |
| Название, символ, номер | Радо́н / Radon (Rn), 86 |
| Атомная масса (молярная масса) | 222,0176 (наиболее стабильный изотоп) а. е. м. (г/моль) |
| Электронная конфигурация | [Xe] 4f14 5d10 6s2 6p6 |
| Радиус атома | 214 пм |
| Химические свойства | |
| Ковалентный радиус | 140—150 пм |
| Степени окисления | +2, +4, +6, +8[1] |
| Энергия ионизации (первый электрон) | 1036,5 (10,74) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | (газ, при 0 °C) 9,81 кг/м3 (жидк., при −62 °C) 4,4 г/см³ |
| Температура плавления | 202 K (−71,15 °C) |
| Температура кипения | 211,4 K (−61,75 °C) |
| Уд. теплота плавления | 2,7 кДж/моль |
| Уд. теплота испарения | 18,1 кДж/моль |
| Молярная теплоёмкость | 20,79[1] Дж/(K·моль) |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая гранецентрированая |
| Прочие характеристики | |
| Теплопроводность | (300 K) (газ, при 0 °C) 0,0036 Вт/(м·К) |
| Номер CAS | 10043-92-2 |
| 86 | Радон |
| 4f145d106s26p6 | |
Радо́н — элемент 18-й группы периодической системы химических элементов Д. И. Менделеева (по старой классификации — главной подгруппы 8-й группы), 6-го периода, с атомным номером 86. Обозначается символом Rn (лат. Radon). Простое вещество радон при нормальных условиях — бесцветный инертный газ; радиоактивен, стабильных изотопов не имеет, может представлять опасность для здоровья и жизни. При комнатной температуре является одним из самых тяжёлых газов. Наиболее стабильный изотоп (222Rn) имеет период полураспада 3,8 суток.
История открытия и происхождение названия
В 1899 году Пьер и Мария Кюри обнаружили, что газ, находившийся в контакте с радием, остаётся радиоактивным в течение месяца[2]. Эрнест Резерфорд и Роберт Оуэнс позже в том же году отметили[3], что радиоактивность препаратов тория колеблется со временем. Позже Резерфорд объяснил это тем, что торий испускает, кроме α-частиц, и некое неизвестное ранее вещество, так что воздух вокруг препаратов тория постепенно становится радиоактивным[4]. Это вещество он предложил назвать эмана́цией (от лат. emanatio «истечение») тория и дать ему символ Em. Последующие наблюдения Резерфорда в 1901 году показали, что и препараты радия также испускают некую эманацию, которая обладает радиоактивными свойствами и ведёт себя как инертный газ[5], однако он в этой работе отметил приоритет супругов Кюри в открытии эманации. В 1903 году французский химик Андре-Луи Дебьерн обнаружил короткоживущую эманацию актиния[6].
Первоначально эманацию тория называли торо́ном, эманацию радия — радо́ном, актиния — актино́ном. Было доказано, что все эманации на самом деле представляют собой радионуклиды нового элемента — инертного газа, которому отвечает атомный номер 86. Впервые его выделили в чистом виде и измерили его плотность Уильям Рамзай и Роберт Уитлоу-Грей в 1908 году[7], они же предложили назвать газ нитон (от лат. nitens, светящийся). В 1923 году газ получил окончательное название радон, и символ Em был сменён на Rn.
В публичной лекции 1936 года Резерфорд кратко изложил итоги их работ:
Я помогал ему [профессору по электротехнике Оуэнсу в университете МакГилл в г. Монреале в Канаде с декабря 1898 года по 26 мая 1899 года] в проведении экспериментов, и мы обнаружили некоторые очень странные явления. Оказалось, что радиоактивное воздействие окиси тория может проходить сквозь дюжину листков бумаги, положенных поверх этой окиси, но задерживается тончайшей пластинкой слюды, как будто излучается что-то, способное диффундировать сквозь поры бумаги. Тот факт, что прибор был очень чувствителен к движению воздуха, поддерживал эту диффузионную гипотезу. Затем мы провели эксперименты, в которых воздух проходил над окисью тория, а потом попадал в ионизационную камеру. Эти опыты показали, что активность может переноситься воздухом. Однако, когда поток воздуха прекращался, активность в ионизационной камере не сразу исчезала, а уменьшалась постепенно по экспоненциальному закону. Я назвал это газообразное вещество, которое может диффундировать сквозь бумагу, переноситься воздухом и в течение некоторого времени сохранять свою активность, исчезающую по характерному закону, «эманацией тория».
Я установил, что эта эманация обладает чрезвычайно своеобразным свойством делать радиоактивными тела, над которыми она проходит. Казалось, что это свойство, скорее всего, обусловлено осаждением некой материальной субстанции, а не какой-либо активностью, возникшей в самих телах под действием излучения, так как тогда количество осаждённого вещества должно увеличиваться при приложении электрического поля. В те времена многие получали неповторяющиеся и странные результаты, помещая предметы вблизи радиоактивных веществ. По-видимому, всё это могло объясняться наличием таких же эманаций, как обнаруженная нами у тория.
Прежде чем считать такое объяснение правильным, необходимо было выяснить истинную природу эманации. Это было очень трудно, так как доступное количество её всегда было очень мало.
Заслуга открытия радона как химического элемента часто приписывается также немецкому химику Фридриху Дорну. Вопросы приоритета в открытии радона рассматриваются в работе Джеймса и Вирджинии Маршалл[8], где показано, что первооткрывателем радона как химического элемента следует считать Резерфорда.
В 1900 году Дорн открыл изотоп радона 222Rn с периодом полураспада 3,823 дня и опубликовал статью[9][10] об этом, сославшись на более раннюю работу Резерфорда. Резерфорд, сперва с Оуэнсом, а затем один в 1899 году работал с другим изотопом 220Rn (тороном), период полураспада которого около 55,6 секунды. Резерфорд не знал о работах немца, так как тот опубликовал свою работу в немецком журнале с небольшим тиражом. Резерфорд не знал немецкого. Дорн совершенно не интересовался радиоактивностью. И только в 1902 году Резерфорд и Содди экспериментально доказали, что эманация — это изотоп радона. Они сумели её охладить и превратить в жидкость с помощью новой физической установки в университете МакГилл и опубликовали статьи.
Нахождение в природе
Входит в состав радиоактивных рядов 238U, 235U и 232Th. Ядра радона постоянно возникают в природе при радиоактивном распаде материнских ядер. Равновесное содержание в земной коре 7·10–16% по массе. Ввиду химической инертности радон относительно легко покидает кристаллическую решётку «родительского» минерала и попадает в подземные воды, природные газы и воздух. Поскольку наиболее долгоживущим из четырёх природных изотопов радона (218, 219, 220, 222) является 222Rn, именно его содержание в этих средах максимально.
Концентрация радона в воздухе зависит, в первую очередь, от геологической обстановки (так, граниты, в которых много урана, являются активными источниками радона, в то же время над поверхностью морей радона мало), а также от погоды (во время дождя микротрещины, по которым радон поступает из почвы, заполняются водой; снежный покров также препятствует доступу радона в воздух).
Перед землетрясениями наблюдается повышение концентрации радона в воздухе, благодаря сейсмической активности[11]. Выход радона из земли в это время называется эксхаляция[12]
Получение
Для получения радона через водный раствор любой соли радия-226 продувают воздух, который уносит с собой радон-222, образующийся при радиоактивном распаде радия-226. Далее воздух тщательно фильтруют для отделения микрокапель раствора, содержащего соль радия, которые могут быть захвачены током воздуха. Для получения собственно радона из смеси газов удаляют химически активные вещества (кислород, водород, водяные пары и т. д.), остаток конденсируют жидким азотом, затем из конденсата отгоняют азот и инертные газы (аргон, неон и т. д.).
В одном грамме радия-226 возникает за сутки около 1 мм3 радона-222.
Физические свойства
Эмиссионный спектр радона, сфотографированный Э. Резерфордом в 1908 году. Числа на краях спектра представляют собой длины волн. Средний спектр принадлежит радону, внешние спектры — гелию (добавлены для калибровки длин волн)Радон — радиоактивный одноатомный тяжёлый газ без цвета и запаха. Растворимость в воде при комнатной температуре составляет 460 мл/л, что выше, чем растворимость более лёгких инертных газов. В органических растворителях и в жировой ткани человека растворимость радона в десятки раз выше, чем в воде. Газ хорошо просачивается сквозь полимерные плёнки. Легко адсорбируется активированным углём и силикагелем.
Собственная радиоактивность радона вызывает его флюоресценцию. Газообразный и жидкий радон флюоресцирует голубым светом, у твёрдого радона при охлаждении до азотных температур цвет флюоресценции становится сперва жёлтым, затем — красно-оранжевым.
Цвет свечения в газовом разряде у радона — синий, так как в видимой части спектра радона особо выделяются 8 линий, отвечающих длинам волн от 3982 до 5085 Å и лежащих главным образом в синей части спектра[13], однако из-за отсутствия стабильных изотопов применение его в газосветных приборах невозможно.
Плотность радона при нормальных условиях составляет 9,73 кг/м3, что примерно в 7,6 раз больше плотности воздуха.
Химические свойства
схема электронных оболочек радонаВ химическом отношении радон является наиболее активным из благородных газов, так как его электроны внешних электронных оболочек имеют относительную низкую энергию ионизации.
Радон образует химические соединения с фтором. Так, дифторид радона RnF2 является белым нелетучим кристаллическим веществом.
Фториды радона могут быть получены также под действием сильных фторирующих агентов (например, фторидов галогенов: ClF3, BrF5, IF7[14]).
Получены также соединения с катионом RnF+: RnF[SbF6], RnF[Sb2F11][14].
Кроме фтора, радон может образовывать бинарные соединения с кислородом; в частности, был получен триоксид радона[15], однако получение других оксидов радона не подтверждено.
Кроме того, радон может входить в состав различных клатратов, которые, хотя и имеют постоянный стехиометрический состав, не образуют химических связей с участием атомов радона.
Применение
Радон используют в медицине для приготовления радоновых ванн (при этом их эффективность научно не доказана[источник не указан 499 дней]). Радон используется в сельском хозяйстве для активации кормов домашних животных[1], в металлургии в качестве индикатора при определении скорости газовых потоков в доменных печах, газопроводах. В геологии измерение содержания радона в воздухе и воде применяется для поиска месторождений урана и тория, а также активных тектонических разломов, на наличие которых может указывать повышенное содержание радона в приземном и подпочвенном воздухе; в гидрогеологии — для исследования взаимодействия грунтовых и речных вод.
Динамика концентрации радона в подземных водах может применяться для прогноза землетрясений[16].
История
Открытие радиоактивности и радона совпало с повышением интереса к биологическим эффектам радиации. Было установлено, что вода многих источников минеральных вод богата эманацией радия (так именовался радон в то время). Вслед за этим открытием последовала волна моды «на радиацию». В частности, в рекламе того времени радиоактивность минеральных вод выдавалась за главный показатель их полезности и эффективности.
Радиационный фон помещений
Радиационный фон помещений зданий (РФП) — излучение земного и космического происхождения постоянно воздействующее на человека при его нахождении в пространстве внутри здания. РФП формируется, как естественный и технологически измененный радиационный фон; обычно причиной возникновения радиационного фона в зданиях является активность трех основных естественных долгоживущих радионуклидов: радий-226, торий-232 и калий-40, а также техногенного цезия-137 в строительных материалах и активность в воздухе короткоживущих изотопов (Т1/2<10 сут) радия и крайне редко тория. Основные составляющие радиационного фона помещений в значительной степени зависят от деятельности человека. Это вызвано, прежде всего, такими факторами, как выбор площадки для строительства, радиационных характеристик строительных материалов, конструктивных решений зданий и применяемых в них систем вентиляции[17][18]. Измерения не всегда подтверждают сложившийся вывод о том, что в подвальных помещениях и на нижних этажах зданий радон скапливается в больших концентрациях, чем на верхних. Безопасной средней по площади здания плотность потока радона на поверхности грунта считается менее 80 мБк/м2с для жилых зданий и 40 мБк/м2с для малоэтажных коттеджей[19].
Биологическое воздействие
Радон радиотоксичен и канцерогенен. Попадая в организм человека, он способствует процессам, приводящим к раку лёгкого. Распад ядер радона и его дочерних изотопов в лёгочной ткани вызывает микроожог, поскольку вся энергия альфа-частиц поглощается практически в точке распада. Особенно опасно (повышает риск заболевания) сочетание воздействия радона и курения. По данным департамента здравоохранения США радон — второй по частоте (после курения) фактор, вызывающий рак лёгких преимущественно бронхогенного (центрального) типа. Рак лёгких, вызванный радоновым облучением, является шестой по частоте причиной смерти от рака[20].
Радон и его дочерние продукты обусловливают более половины всей эффективной дозы облучения, которую в среднем получает организм человека от природных и техногенных радионуклидов окружающей среды.
В настоящее время во многих странах проведен мониторинг концентрации радона в зданиях как первый этап оптимизации защиты населения[21].
МКРЗ установила референтный уровень объемной активности радона в жилище на уровне 300 Бк/куб.м.[22]
Тестирование и снижение уровня радона
| Этот раздел описывает ситуацию применительно лишь к одному региону, возможно, нарушая при этом правило о взвешенности изложения. Вы можете помочь Википедии, добавив информацию для других стран и регионов. |
Существуют достаточно простые тесты, позволяющие измерить уровень радона. В некоторых странах такие тесты методически проводятся в местах, где систематически наблюдаются угрозы. Устройства для измерения уровня радона имеются в продаже. Цифровые устройства для измерения радона позволяют проводить текущие измерения, производящие ежедневные, еженедельные, краткосрочные и долгосрочные отчеты с помощью цифрового дисплея. Устройства для краткосрочного первоначального тестирования уровня радона недороги, и в некоторых случаях бесплатны. Существуют строгие правила проведения краткосрочных тестов, и их соблюдение крайне важно. Комплект для измерения уровня радона включает в себя коллектор, который необходимо повесить на нижнем этаже жилого дома на период от 2х до 7 дней. Далее пользователю необходимо отправить коллектор в лабораторию для анализа. Также доступны приборы для долгосрочного (на срок до одного года) измерения уровня радона. Есть возможность измерения количества выделяемого из земли радона до начала строительства [23]. Концентрация радона может меняться ежедневно, поэтому необходимы долгосрочные измерения средней концентрации радона в помещениях, где человек проводит значительную часть времени [24].
Концентрация радона подвержена естественным колебаниям из-за таких факторов, как смена погодных условий, поэтому первоначальный тест может дать неточный результат относительно средней концентрации радона. Уровень радона в воздухе максимален в наиболее холодной части дня, когда перепады давления наиболее велики[25]. Поэтому при обнаружении высокой концентрации радона (более 4 pCi/L) оправдано проведение повторных измерений перед осуществлением более дорогостоящих мероприятий по борьбе с выделением газа. Показания в промежутке от 4 до 10 pCi/L являются показанием к проведению долгосрочного теста. Показания выше 10 pCi/L требуют только дополнительного краткосрочного теста, дабы избежать чрезмерного промедления в борьбе с выделением газа. Покупателям недвижимости рекомендуется отложить или отказаться от покупки, если продавец не смог снизить уровень радона до 4 pCi/L или менее[23].
Поскольку период полураспада радона составляет всего 3,8 дней, удаление или изоляция источника значительно снижает угрозу в течение нескольких недель. Также можно снизить концентрацию радона с помощью изменения вентилирования сооружения. Концентрация радона, как правило, снижается при вентиляции помещения[26]. В хорошо проветриваемых помещениях концентрация радона имеет тенденцию выравниваться до уровня улицы (обычно 10 Бк/м3, в пределах от 1 до 100 Бк/м3)[23].
Есть четыре основных способа снизить концентрацию радона в домах[23][27]:
- Разгерметизация (всасывание почвы) за счет увеличения вентилирования между этажами
- Улучшение вентиляции помещения и предотвращение проникновения радона из подвальных помещений в жилые помещения
- Установка системы для удаления радона из подвальных помещений
- Установка систем вентиляции с положительным давлением
Согласно EPA[23], для уменьшения концентрации радона в первую очередь используются система труб дефлектора и вентилятор, высасывающие радон из-под дома наружу. Концентрация радона в помещении, как правило, может быть уменьшена с помощью разгерметизации и перенаправления загрязненного радоном воздуха в открытое пространство, вдалеке от окон и строительных отверстий. EPA рекомендует использовать методы, препятствующие проникновения радона в помещение. Всасывание почвы, например, предотвращает появление радона в доме, потому что радон из-под дома выпускается наружу через трубы, где он разбавляется[28]. EPA не рекомендует использовать герметизацию без других мер, поскольку использование такого метода не приводит к значительным и последовательным снижениям уровня радона[28].
Система вентиляции с положительным давлением может быть объединена с теплообменником для восстановления энергии в процессе воздухообмена с воздухом извне, поскольку исключительно выведение воздуха наружу может быть недостаточным решением, так как это может привести к всасыванию воздуха в жилище. В дома, построенные над погребами, можно установить листы пластика, покрывающие пустое пространство — это будет барьером для радона [23]. Вентиляционная труба и вентилятор используются для выведения радона из-под пласта пластика на открытый воздух. Этот способ выведения радона называется «подмембранное всасывание», и при правильном применении оно является самым эффективным способом выведения радона в домах с погребным помещением[24].
Изотопы
Радон не имеет стабильных изотопов. Наиболее устойчив 222Rn (T1/2=3,8235 суток), входящий в природное радиоактивное семейство урана-238 (семейство урана-радия) и являющийся непосредственным продуктом распада радия-226. Иногда название «радон» относят именно к этому изотопу. В семейство тория-232 входит 220Rn (T1/2=55,6 с), иногда его называют торон (Tn). В семейство урана-235 (урана-актиния) входит 219Rn (T1/2=3,96 с), его называют актинон (An). В одну из побочных ветвей (коэффициент ветвления 2·10−7) семейства урана-радия входит также очень короткоживущий (T1/2=35 мс) радон-218. Все отмеченные изотопы радона испытывают альфа-распад. Этими четырьмя нуклидами исчерпывается список природных изотопов радона. Известны ещё 30 искусственных изотопов Rn с массовым числом от 195 до 228. Некоторые нейтронодефицитные изотопы радона имеют также возбуждённые метастабильные состояния; таких состояний известно 13. Преобладающие моды распада у лёгких изотопов Rn — альфа-распад, позитронный распад и электронный захват. Начиная с массового числа A=212 альфа-распад становится доминирующим. Тяжёлые изотопы радона (начиная с A=223) распадаются преимущественно посредством бета-минус-распада.
Примечания
- ↑ 1 2 3 Химическая энциклопедия / Редкол.: Кнунянц И. Л. и др.. — М.: Советская энциклопедия, 1995. — Т. 4 (Пол-Три). — 639 с. — ISBN 5-82270-092-4.
- ↑ P.Curie, Mme. Marie Curie (1899). «Sur la radioactivite provoquee par les rayons de Becquerel». Comptes rendus hebdomadaires des séances de l’Académie des sciences 129: 714–716.
- ↑ E. Rutherford, R. B. Owens (1899). «Thorium and uranium radiation». Trans. R. Soc. Can. 2: 9–12.
- ↑ Rutherford, E. (1900). «A radioactive substance emitted from thorium compounds». Phil. Mag. 40: 1–4.
- ↑ E. Rutherford, H.T. Brooks (1901). «The new gas from radium». Trans. R. Soc. Can. 7: 21–25.
- ↑ Debierne, André-Louis (1903). «Sur la radioactivite induite provoquee par les sels d’actinium». Comptes rendus hebdomadaires des seances de l’Academie des sciences 136.
- ↑ W.Ramsay, R. W. Gray (1910). «La densité de l’emanation du radium». Comptes rendus hebdomadaires des seances de l’Academie des sciences 151: 126–128.
- ↑ James L. Marshall and Virginia R. Marshall (2003). «ERNEST RUTHERFORD, THE «TRUE DISCOVERER» OF RADON». Bulletin for the History of Chemistry 28 (2): 76-83.
- ↑ Dorn, Friedrich Ernst (1900). «Ueber die von radioaktiven Substanzen ausgesandte Emanation». Abhandlungen der Naturforschenden Gesellschaft zu Halle 22.
- ↑ Dorn, F. E. (1900). «Die von radioactiven Substanzen ausgesandte Emanation». Abhandlungen der Naturforschenden Gesellschaft zu Halle 23: 1–15.
- ↑ Уткин В. И., Юрков А. К. Радон как «детерминированный» индикатор природных и техногенных геодинамических процессов // Доклады РАН. 2009. Т. 426. № 6. С. 816—820.
- ↑ Уткин В. И., Юрков А. К. Отражение сейсмических событий в поле эксхаляции радона // Геофизика. 1997. № 6. С. 50-56.
- ↑ Михайленко Я. И. Курс общей и неорганической химии. — 1966. — С. 635. — 664 с.
- ↑ 1 2 Леонтьев А. В., Фомичева О. А., Проскурнина М. В., Зефиров Н. С. (1982). «Современное состояние химии радона». Успехи химии 51 (1): 23-39.
- ↑ A. G. Sykes. Recent Advances in Noble-Gas Chemistry // Advances in Inorganic Chemistry. — Academic Press, 1998. — Vol. 46. — P. 91–93. — ISBN 978-0120236466.
- ↑ Уткин В. И., Юрков А. К. Динамика выделения радона из массива горных пород как краткосрочный предвестник землетрясения // Докл. РАН. 1998. Т. 358. № 5. С. 675-680.
- ↑ Крисюк, Э.М. Радиационный фон помещений. — М.: Энергоатомиздат, 1989. — 120 с. — ISBN 5-283-02992-1.
- ↑ Р. А. Назиров, Е.В. Пересыпкин, И.В. Тарасов, В.И. Верещагин. Снижение естественной радиоактивности цементных бетонов // Известия высших учебных заведений. Строительство : науч. — теоретич. журн./ М-во высш. и сред. специального образования РФ, Ассоц. строит. вузов СНГ, Новосиб. гос. архитектурно — строит. ун-т. : журнал. — 2007. — Январь (№ 1). — С. 45—49. — ISSN 0536-1052.
- ↑ Таблица № 2 ТСН РБ-2003 МО
- ↑ S. Darby, D. Hill, R. Doll (2001). «Radon: A likely carcinogen at all exposures». Annals of Oncology 12 (10): 27. DOI:10.1023/A:1012518223463.
- ↑ WHO Handbook on Indoor Radon: A Public Health Perspective. — Geneva: World Health Organization, 2009-01-01. — (WHO Guidelines Approved by the Guidelines Review Committee). — ISBN 9789241547673.
- ↑ M. Tirmarche, J. D. Harrison, D. Laurier, F. Paquet, E. Blanchardon. ICRP Publication 115. Lung cancer risk from radon and progeny and statement on radon // Annals of the ICRP. — 2010-02-01. — Т. 40, вып. 1. — С. 1–64. — ISSN 1872-969X. — DOI:10.1016/j.icrp.2011.08.011.
- ↑ 1 2 3 4 5 6 United States Environmental Protection Agency. «A Citizen’s Guide to Radon».
- ↑ 1 2 Baes, Fred. Environmental and Background Radiation — Radon.
- ↑ Thad. Godish, (2001) . «Indoor Environment Quality». Boca Raton, FL. CRC Press LLC.
- ↑ Agency for Toxic Substances and Disease Registry, U.S. Public Health Service, In collaboration with U.S. Environmental Protection Agency. Toxicological profile for radon.
- ↑ World Health Organization. Radon and cancer, fact sheet 291.
- ↑ 1 2 Consumer’s Guide to Radon Reduction: How to fix your home.
Ссылки
Радон — Википедия. Что такое Радон
| Внешний вид простого вещества | |
|---|---|
Бесцветный, слегка флюоресцирующий радиоактивный газ | |
| Свойства атома | |
| Название, символ, номер | Радо́н / Radon (Rn), 86 |
| Атомная масса (молярная масса) | 222,0176 (наиболее стабильный изотоп) а. е. м. (г/моль) |
| Электронная конфигурация | [Xe] 4f14 5d10 6s2 6p6 |
| Радиус атома | 214 пм |
| Химические свойства | |
| Ковалентный радиус | 140—150 пм |
| Степени окисления | +2, +4, +6, +8[1] |
| Энергия ионизации (первый электрон) | 1036,5 (10,74) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | (газ, при 0 °C) 9,81 кг/м3 (жидк., при −62 °C) 4,4 г/см³ |
| Температура плавления | 202 K (−71,15 °C) |
| Температура кипения | 211,4 K (−61,75 °C) |
| Уд. теплота плавления | 2,7 кДж/моль |
| Уд. теплота испарения | 18,1 кДж/моль |
| Молярная теплоёмкость | 20,79[1] Дж/(K·моль) |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая гранецентрированая |
| Прочие характеристики | |
| Теплопроводность | (300 K) (газ, при 0 °C) 0,0036 Вт/(м·К) |
| Номер CAS | 10043-92-2 |
| 86 | Радон |
| 4f145d106s26p6 | |
Радо́н — элемент 18-й группы периодической системы химических элементов Д. И. Менделеева (по старой классификации — главной подгруппы 8-й группы), 6-го периода, с атомным номером 86. Обозначается символом Rn (лат. Radon). Простое вещество радон при нормальных условиях — бесцветный инертный газ; радиоактивен, стабильных изотопов не имеет, может представлять опасность для здоровья и жизни. При комнатной температуре является одним из самых тяжёлых газов. Наиболее стабильный изотоп (222Rn) имеет период полураспада 3,8 суток.
История открытия и происхождение названия
В 1899 году Пьер и Мария Кюри обнаружили, что газ, находившийся в контакте с радием, остаётся радиоактивным в течение месяца[2]. Эрнест Резерфорд и Роберт Оуэнс позже в том же году отметили[3], что радиоактивность препаратов тория колеблется со временем. Позже Резерфорд объяснил это тем, что торий испускает, кроме α-частиц, и некое неизвестное ранее вещество, так что воздух вокруг препаратов тория постепенно становится радиоактивным[4]. Это вещество он предложил назвать эмана́цией (от лат. emanatio «истечение») тория и дать ему символ Em. Последующие наблюдения Резерфорда в 1901 году показали, что и препараты радия также испускают некую эманацию, которая обладает радиоактивными свойствами и ведёт себя как инертный газ[5], однако он в этой работе отметил приоритет супругов Кюри в открытии эманации. В 1903 году французский химик Андре-Луи Дебьерн обнаружил короткоживущую эманацию актиния[6].
Первоначально эманацию тория называли торо́ном, эманацию радия — радо́ном, актиния — актино́ном. Было доказано, что все эманации на самом деле представляют собой радионуклиды нового элемента — инертного газа, которому отвечает атомный номер 86. Впервые его выделили в чистом виде и измерили его плотность Уильям Рамзай и Роберт Уитлоу-Грей в 1908 году[7], они же предложили назвать газ нитон (от лат. nitens, светящийся). В 1923 году газ получил окончательное название радон, и символ Em был сменён на Rn.
В публичной лекции 1936 года Резерфорд кратко изложил итоги их работ:
Я помогал ему [профессору по электротехнике Оуэнсу в университете МакГилл в г. Монреале в Канаде с декабря 1898 года по 26 мая 1899 года] в проведении экспериментов, и мы обнаружили некоторые очень странные явления. Оказалось, что радиоактивное воздействие окиси тория может проходить сквозь дюжину листков бумаги, положенных поверх этой окиси, но задерживается тончайшей пластинкой слюды, как будто излучается что-то, способное диффундировать сквозь поры бумаги. Тот факт, что прибор был очень чувствителен к движению воздуха, поддерживал эту диффузионную гипотезу. Затем мы провели эксперименты, в которых воздух проходил над окисью тория, а потом попадал в ионизационную камеру. Эти опыты показали, что активность может переноситься воздухом. Однако, когда поток воздуха прекращался, активность в ионизационной камере не сразу исчезала, а уменьшалась постепенно по экспоненциальному закону. Я назвал это газообразное вещество, которое может диффундировать сквозь бумагу, переноситься воздухом и в течение некоторого времени сохранять свою активность, исчезающую по характерному закону, «эманацией тория».
Я установил, что эта эманация обладает чрезвычайно своеобразным свойством делать радиоактивными тела, над которыми она проходит. Казалось, что это свойство, скорее всего, обусловлено осаждением некой материальной субстанции, а не какой-либо активностью, возникшей в самих телах под действием излучения, так как тогда количество осаждённого вещества должно увеличиваться при приложении электрического поля. В те времена многие получали неповторяющиеся и странные результаты, помещая предметы вблизи радиоактивных веществ. По-видимому, всё это могло объясняться наличием таких же эманаций, как обнаруженная нами у тория.
Прежде чем считать такое объяснение правильным, необходимо было выяснить истинную природу эманации. Это было очень трудно, так как доступное количество её всегда было очень мало.
Заслуга открытия радона как химического элемента часто приписывается также немецкому химику Фридриху Дорну. Вопросы приоритета в открытии радона рассматриваются в работе Джеймса и Вирджинии Маршалл[8], где показано, что первооткрывателем радона как химического элемента следует считать Резерфорда.
В 1900 году Дорн открыл изотоп радона 222Rn с периодом полураспада 3,823 дня и опубликовал статью[9][10] об этом, сославшись на более раннюю работу Резерфорда. Резерфорд, сперва с Оуэнсом, а затем один в 1899 году работал с другим изотопом 220Rn (тороном), период полураспада которого около 55,6 секунды. Резерфорд не знал о работах немца, так как тот опубликовал свою работу в немецком журнале с небольшим тиражом. Резерфорд не знал немецкого. Дорн совершенно не интересовался радиоактивностью. И только в 1902 году Резерфорд и Содди экспериментально доказали, что эманация — это изотоп радона. Они сумели её охладить и превратить в жидкость с помощью новой физической установки в университете МакГилл и опубликовали статьи.
Нахождение в природе

Входит в состав радиоактивных рядов 238U, 235U и 232Th. Ядра радона постоянно возникают в природе при радиоактивном распаде материнских ядер. Равновесное содержание в земной коре 7·10–16% по массе. Ввиду химической инертности радон относительно легко покидает кристаллическую решётку «родительского» минерала и попадает в подземные воды, природные газы и воздух. Поскольку наиболее долгоживущим из четырёх природных изотопов радона (218, 219, 220, 222) является 222Rn, именно его содержание в этих средах максимально.
Концентрация радона в воздухе зависит, в первую очередь, от геологической обстановки (так, граниты, в которых много урана, являются активными источниками радона, в то же время над поверхностью морей радона мало), а также от погоды (во время дождя микротрещины, по которым радон поступает из почвы, заполняются водой; снежный покров также препятствует доступу радона в воздух).
Перед землетрясениями наблюдается повышение концентрации радона в воздухе, благодаря сейсмической активности[11]. Выход радона из земли в это время называется эксхаляция[12]
Получение
Для получения радона через водный раствор любой соли радия-226 продувают воздух, который уносит с собой радон-222, образующийся при радиоактивном распаде радия-226. Далее воздух тщательно фильтруют для отделения микрокапель раствора, содержащего соль радия, которые могут быть захвачены током воздуха. Для получения собственно радона из смеси газов удаляют химически активные вещества (кислород, водород, водяные пары и т. д.), остаток конденсируют жидким азотом, затем из конденсата отгоняют азот и инертные газы (аргон, неон и т. д.).
В одном грамме радия-226 возникает за сутки около 1 мм3 радона-222.
Физические свойства
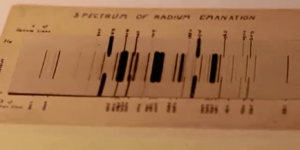 Эмиссионный спектр радона, сфотографированный Э. Резерфордом в 1908 году. Числа на краях спектра представляют собой длины волн. Средний спектр принадлежит радону, внешние спектры — гелию (добавлены для калибровки длин волн)
Эмиссионный спектр радона, сфотографированный Э. Резерфордом в 1908 году. Числа на краях спектра представляют собой длины волн. Средний спектр принадлежит радону, внешние спектры — гелию (добавлены для калибровки длин волн)Радон — радиоактивный одноатомный тяжёлый газ без цвета и запаха. Растворимость в воде при комнатной температуре составляет 460 мл/л, что выше, чем растворимость более лёгких инертных газов. В органических растворителях и в жировой ткани человека растворимость радона в десятки раз выше, чем в воде. Газ хорошо просачивается сквозь полимерные плёнки. Легко адсорбируется активированным углём и силикагелем.
Собственная радиоактивность радона вызывает его флюоресценцию. Газообразный и жидкий радон флюоресцирует голубым светом, у твёрдого радона при охлаждении до азотных температур цвет флюоресценции становится сперва жёлтым, затем — красно-оранжевым.
Цвет свечения в газовом разряде у радона — синий, так как в видимой части спектра радона особо выделяются 8 линий, отвечающих длинам волн от 3982 до 5085 Å и лежащих главным образом в синей части спектра[13], однако из-за отсутствия стабильных изотопов применение его в газосветных приборах невозможно.
Плотность радона при нормальных условиях составляет 9,73 кг/м3, что примерно в 7,6 раз больше плотности воздуха.
Химические свойства
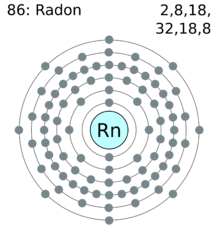 схема электронных оболочек радона
схема электронных оболочек радонаВ химическом отношении радон является наиболее активным из благородных газов, так как его электроны внешних электронных оболочек имеют относительную низкую энергию ионизации.
Радон образует химические соединения с фтором. Так, дифторид радона RnF2 является белым нелетучим кристаллическим веществом.
Фториды радона могут быть получены также под действием сильных фторирующих агентов (например, фторидов галогенов: ClF3, BrF5, IF7[14]).
Получены также соединения с катионом RnF+: RnF[SbF6], RnF[Sb2F11][14].
Кроме фтора, радон может образовывать бинарные соединения с кислородом; в частности, был получен триоксид радона[15], однако получение других оксидов радона не подтверждено.
Кроме того, радон может входить в состав различных клатратов, которые, хотя и имеют постоянный стехиометрический состав, не образуют химических связей с участием атомов радона.
Применение
Радон используют в медицине для приготовления радоновых ванн (при этом их эффективность научно не доказана[источник не указан 491 день]). Радон используется в сельском хозяйстве для активации кормов домашних животных[1], в металлургии в качестве индикатора при определении скорости газовых потоков в доменных печах, газопроводах. В геологии измерение содержания радона в воздухе и воде применяется для поиска месторождений урана и тория, а также активных тектонических разломов, на наличие которых может указывать повышенное содержание радона в приземном и подпочвенном воздухе; в гидрогеологии — для исследования взаимодействия грунтовых и речных вод.
Динамика концентрации радона в подземных водах может применяться для прогноза землетрясений[16].
История
Открытие радиоактивности и радона совпало с повышением интереса к биологическим эффектам радиации. Было установлено, что вода многих источников минеральных вод богата эманацией радия (так именовался радон в то время). Вслед за этим открытием последовала волна моды «на радиацию». В частности, в рекламе того времени радиоактивность минеральных вод выдавалась за главный показатель их полезности и эффективности.
Радиационный фон помещений
Радиационный фон помещений зданий (РФП) — излучение земного и космического происхождения постоянно воздействующее на человека при его нахождении в пространстве внутри здания. РФП формируется, как естественный и технологически измененный радиационный фон; обычно причиной возникновения радиационного фона в зданиях является активность трех основных естественных долгоживущих радионуклидов: радий-226, торий-232 и калий-40, а также техногенного цезия-137 в строительных материалах и активность в воздухе короткоживущих изотопов (Т1/2<10 сут) радия и крайне редко тория. Основные составляющие радиационного фона помещений в значительной степени зависят от деятельности человека. Это вызвано, прежде всего, такими факторами, как выбор площадки для строительства, радиационных характеристик строительных материалов, конструктивных решений зданий и применяемых в них систем вентиляции[17][18]. Измерения не всегда подтверждают сложившийся вывод о том, что в подвальных помещениях и на нижних этажах зданий радон скапливается в больших концентрациях, чем на верхних. Безопасной средней по площади здания плотность потока радона на поверхности грунта считается менее 80 мБк/м2с для жилых зданий и 40 мБк/м2с для малоэтажных коттеджей[19].
Биологическое воздействие
Радон радиотоксичен и канцерогенен. Попадая в организм человека, он способствует процессам, приводящим к раку лёгкого. Распад ядер радона и его дочерних изотопов в лёгочной ткани вызывает микроожог, поскольку вся энергия альфа-частиц поглощается практически в точке распада. Особенно опасно (повышает риск заболевания) сочетание воздействия радона и курения. По данным департамента здравоохранения США радон — второй по частоте (после курения) фактор, вызывающий рак лёгких преимущественно бронхогенного (центрального) типа. Рак лёгких, вызванный радоновым облучением, является шестой по частоте причиной смерти от рака[20].
Радон и его дочерние продукты обусловливают более половины всей эффективной дозы облучения, которую в среднем получает организм человека от природных и техногенных радионуклидов окружающей среды.
В настоящее время во многих странах проведен мониторинг концентрации радона в зданиях как первый этап оптимизации защиты населения[21].
МКРЗ установила референтный уровень объемной активности радона в жилище на уровне 300 Бк/куб.м.[22]
Тестирование и снижение уровня радона
 | Этот раздел описывает ситуацию применительно лишь к одному региону, возможно, нарушая при этом правило о взвешенности изложения. Вы можете помочь Википедии, добавив информацию для других стран и регионов. |
 Цифровой измеритель уровня радона
Цифровой измеритель уровня радонаСуществуют достаточно простые тесты, позволяющие измерить уровень радона. В некоторых странах такие тесты методически проводятся в местах, где систематически наблюдаются угрозы. Устройства для измерения уровня радона имеются в продаже. Цифровые устройства для измерения радона позволяют проводить текущие измерения, производящие ежедневные, еженедельные, краткосрочные и долгосрочные отчеты с помощью цифрового дисплея. Устройства для краткосрочного первоначального тестирования уровня радона недороги, и в некоторых случаях бесплатны. Существуют строгие правила проведения краткосрочных тестов, и их соблюдение крайне важно. Комплект для измерения уровня радона включает в себя коллектор, который необходимо повесить на нижнем этаже жилого дома на период от 2х до 7 дней. Далее пользователю необходимо отправить коллектор в лабораторию для анализа. Также доступны приборы для долгосрочного (на срок до одного года) измерения уровня радона. Есть возможность измерения количества выделяемого из земли радона до начала строительства [23]. Концентрация радона может меняться ежедневно, поэтому необходимы долгосрочные измерения средней концентрации радона в помещениях, где человек проводит значительную часть времени [24].
Концентрация радона подвержена естественным колебаниям из-за таких факторов, как смена погодных условий, поэтому первоначальный тест может дать неточный результат относительно средней концентрации радона. Уровень радона в воздухе максимален в наиболее холодной части дня, когда перепады давления наиболее велики[25]. Поэтому при обнаружении высокой концентрации радона (более 4 pCi/L) оправдано проведение повторных измерений перед осуществлением более дорогостоящих мероприятий по борьбе с выделением газа. Показания в промежутке от 4 до 10 pCi/L являются показанием к проведению долгосрочного теста. Показания выше 10 pCi/L требуют только дополнительного краткосрочного теста, дабы избежать чрезмерного промедления в борьбе с выделением газа. Покупателям недвижимости рекомендуется отложить или отказаться от покупки, если продавец не смог снизить уровень радона до 4 pCi/L или менее[23].
Поскольку период полураспада радона составляет всего 3,8 дней, удаление или изоляция источника значительно снижает угрозу в течение нескольких недель. Также можно снизить концентрацию радона с помощью изменения вентилирования сооружения. Концентрация радона, как правило, снижается при вентиляции помещения[26]. В хорошо проветриваемых помещениях концентрация радона имеет тенденцию выравниваться до уровня улицы (обычно 10 Бк/м3, в пределах от 1 до 100 Бк/м3)[23].
Есть четыре основных способа снизить концентрацию радона в домах[23][27]:
- Разгерметизация (всасывание почвы) за счет увеличения вентилирования между этажами
- Улучшение вентиляции помещения и предотвращение проникновения радона из подвальных помещений в жилые помещения
- Установка системы для удаления радона из подвальных помещений
- Установка систем вентиляции с положительным давлением
Согласно EPA[23], для уменьшения концентрации радона в первую очередь используются система труб дефлектора и вентилятор, высасывающие радон из-под дома наружу. Концентрация радона в помещении, как правило, может быть уменьшена с помощью разгерметизации и перенаправления загрязненного радоном воздуха в открытое пространство, вдалеке от окон и строительных отверстий. EPA рекомендует использовать методы, препятствующие проникновения радона в помещение. Всасывание почвы, например, предотвращает появление радона в доме, потому что радон из-под дома выпускается наружу через трубы, где он разбавляется[28]. EPA не рекомендует использовать герметизацию без других мер, поскольку использование такого метода не приводит к значительным и последовательным снижениям уровня радона[28].
Система вентиляции с положительным давлением может быть объединена с теплообменником для восстановления энергии в процессе воздухообмена с воздухом извне, поскольку исключительно выведение воздуха наружу может быть недостаточным решением, так как это может привести к всасыванию воздуха в жилище. В дома, построенные над погребами, можно установить листы пластика, покрывающие пустое пространство — это будет барьером для радона [23]. Вентиляционная труба и вентилятор используются для выведения радона из-под пласта пластика на открытый воздух. Этот способ выведения радона называется «подмембранное всасывание», и при правильном применении оно является самым эффективным способом выведения радона в домах с погребным помещением[24].
Изотопы
Радон не имеет стабильных изотопов. Наиболее устойчив 222Rn (T1/2=3,8235 суток), входящий в природное радиоактивное семейство урана-238 (семейство урана-радия) и являющийся непосредственным продуктом распада радия-226. Иногда название «радон» относят именно к этому изотопу. В семейство тория-232 входит 220Rn (T1/2=55,6 с), иногда его называют торон (Tn). В семейство урана-235 (урана-актиния) входит 219Rn (T1/2=3,96 с), его называют актинон (An). В одну из побочных ветвей (коэффициент ветвления 2·10−7) семейства урана-радия входит также очень короткоживущий (T1/2=35 мс) радон-218. Все отмеченные изотопы радона испытывают альфа-распад. Этими четырьмя нуклидами исчерпывается список природных изотопов радона. Известны ещё 30 искусственных изотопов Rn с массовым числом от 195 до 228. Некоторые нейтронодефицитные изотопы радона имеют также возбуждённые метастабильные состояния; таких состояний известно 13. Преобладающие моды распада у лёгких изотопов Rn — альфа-распад, позитронный распад и электронный захват. Начиная с массового числа A=212 альфа-распад становится доминирующим. Тяжёлые изотопы радона (начиная с A=223) распадаются преимущественно посредством бета-минус-распада.
Примечания
- ↑ 1 2 3 Химическая энциклопедия / Редкол.: Кнунянц И. Л. и др.. — М.: Советская энциклопедия, 1995. — Т. 4 (Пол-Три). — 639 с. — ISBN 5-82270-092-4.
- ↑ P.Curie, Mme. Marie Curie (1899). «Sur la radioactivite provoquee par les rayons de Becquerel». Comptes rendus hebdomadaires des séances de l’Académie des sciences 129: 714–716.
- ↑ E. Rutherford, R. B. Owens (1899). «Thorium and uranium radiation». Trans. R. Soc. Can. 2: 9–12.
- ↑ Rutherford, E. (1900). «A radioactive substance emitted from thorium compounds». Phil. Mag. 40: 1–4.
- ↑ E. Rutherford, H.T. Brooks (1901). «The new gas from radium». Trans. R. Soc. Can. 7: 21–25.
- ↑ Debierne, André-Louis (1903). «Sur la radioactivite induite provoquee par les sels d’actinium». Comptes rendus hebdomadaires des seances de l’Academie des sciences 136.
- ↑ W.Ramsay, R. W. Gray (1910). «La densité de l’emanation du radium». Comptes rendus hebdomadaires des seances de l’Academie des sciences 151: 126–128.
- ↑ James L. Marshall and Virginia R. Marshall (2003). «ERNEST RUTHERFORD, THE «TRUE DISCOVERER» OF RADON». Bulletin for the History of Chemistry 28 (2): 76-83.
- ↑ Dorn, Friedrich Ernst (1900). «Ueber die von radioaktiven Substanzen ausgesandte Emanation». Abhandlungen der Naturforschenden Gesellschaft zu Halle 22.
- ↑ Dorn, F. E. (1900). «Die von radioactiven Substanzen ausgesandte Emanation». Abhandlungen der Naturforschenden Gesellschaft zu Halle 23: 1–15.
- ↑ Уткин В. И., Юрков А. К. Радон как «детерминированный» индикатор природных и техногенных геодинамических процессов // Доклады РАН. 2009. Т. 426. № 6. С. 816—820.
- ↑ Уткин В. И., Юрков А. К. Отражение сейсмических событий в поле эксхаляции радона // Геофизика. 1997. № 6. С. 50-56.
- ↑ Михайленко Я. И. Курс общей и неорганической химии. — 1966. — С. 635. — 664 с.
- ↑ 1 2 Леонтьев А. В., Фомичева О. А., Проскурнина М. В., Зефиров Н. С. (1982). «Современное состояние химии радона». Успехи химии 51 (1): 23-39.
- ↑ A. G. Sykes. Recent Advances in Noble-Gas Chemistry // Advances in Inorganic Chemistry. — Academic Press, 1998. — Vol. 46. — P. 91–93. — ISBN 978-0120236466.
- ↑ Уткин В. И., Юрков А. К. Динамика выделения радона из массива горных пород как краткосрочный предвестник землетрясения // Докл. РАН. 1998. Т. 358. № 5. С. 675-680.
- ↑ Крисюк, Э.М. Радиационный фон помещений. — М.: Энергоатомиздат, 1989. — 120 с. — ISBN 5-283-02992-1.
- ↑ Р. А. Назиров, Е.В. Пересыпкин, И.В. Тарасов, В.И. Верещагин. Снижение естественной радиоактивности цементных бетонов // Известия высших учебных заведений. Строительство : науч. — теоретич. журн./ М-во высш. и сред. специального образования РФ, Ассоц. строит. вузов СНГ, Новосиб. гос. архитектурно — строит. ун-т. : журнал. — 2007. — Январь (№ 1). — С. 45—49. — ISSN 0536-1052.
- ↑ Таблица № 2 ТСН РБ-2003 МО
- ↑ S. Darby, D. Hill, R. Doll (2001). «Radon: A likely carcinogen at all exposures». Annals of Oncology 12 (10): 27. DOI:10.1023/A:1012518223463.
- ↑ WHO Handbook on Indoor Radon: A Public Health Perspective. — Geneva: World Health Organization, 2009-01-01. — (WHO Guidelines Approved by the Guidelines Review Committee). — ISBN 9789241547673.
- ↑ M. Tirmarche, J. D. Harrison, D. Laurier, F. Paquet, E. Blanchardon. ICRP Publication 115. Lung cancer risk from radon and progeny and statement on radon // Annals of the ICRP. — 2010-02-01. — Т. 40, вып. 1. — С. 1–64. — ISSN 1872-969X. — DOI:10.1016/j.icrp.2011.08.011.
- ↑ 1 2 3 4 5 6 United States Environmental Protection Agency. «A Citizen’s Guide to Radon».
- ↑ 1 2 Baes, Fred. Environmental and Background Radiation — Radon.
- ↑ Thad. Godish, (2001) . «Indoor Environment Quality». Boca Raton, FL. CRC Press LLC.
- ↑ Agency for Toxic Substances and Disease Registry, U.S. Public Health Service, In collaboration with U.S. Environmental Protection Agency. Toxicological profile for radon.
- ↑ World Health Organization. Radon and cancer, fact sheet 291.
- ↑ 1 2 Consumer’s Guide to Radon Reduction: How to fix your home.
Ссылки
Радон — Википедия
| Внешний вид простого вещества | |
|---|---|
Бесцветный, слегка флюоресцирующий радиоактивный газ | |
| Свойства атома | |
| Название, символ, номер | Радо́н / Radon (Rn), 86 |
| Атомная масса (молярная масса) | 222,0176 (наиболее стабильный изотоп) а. е. м. (г/моль) |
| Электронная конфигурация | [Xe] 4f14 5d10 6s2 6p6 |
| Радиус атома | 214 пм |
| Химические свойства | |
| Ковалентный радиус | 140—150 пм |
| Степени окисления | +2, +4, +6, +8[1] |
| Энергия ионизации (первый электрон) | 1036,5 (10,74) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | (газ, при 0 °C) 9,81 кг/м3 (жидк., при −62 °C) 4,4 г/см³ |
| Температура плавления | 202 K (−71,15 °C) |
| Температура кипения | 211,4 K (−61,75 °C) |
| Уд. теплота плавления | 2,7 кДж/моль |
| Уд. теплота испарения | 18,1 кДж/моль |
| Молярная теплоёмкость | 20,79[1] Дж/(K·моль) |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая гранецентрированая |
| Прочие характеристики | |
| Теплопроводность | (300 K) (газ, при 0 °C) 0,0036 Вт/(м·К) |
| Номер CAS | 10043-92-2 |
| 86 | Радон |
| 4f145d106s26p6 | |
Радо́н — элемент 18-й группы периодической системы химических элементов Д. И. Менделеева (по старой классификации — главной подгруппы 8-й группы), 6-го периода, с атомным номером 86. Обозначается символом Rn (лат. Radon). Простое вещество радон при нормальных условиях — бесцветный инертный газ; радиоактивен, стабильных изотопов не имеет, может представлять опасность для здоровья и жизни. При комнатной температуре является одним из самых тяжёлых газов. Наиболее стабильный изотоп (222Rn) имеет период полураспада 3,8 суток.
История открытия и происхождение названия
В 1899 году Пьер и Мария Кюри обнаружили, что газ, находившийся в контакте с радием, остаётся радиоактивным в течение месяца[2]. Эрнест Резерфорд и Роберт Оуэнс позже в том же году отметили[3], что радиоактивность препаратов тория колеблется со временем. Позже Резерфорд объяснил это тем, что торий испускает, кроме α-частиц, и некое неизвестное ранее вещество, так что воздух вокруг препаратов тория постепенно становится радиоактивным[4]. Это вещество он предложил назвать эмана́цией (от лат. emanatio «истечение») тория и дать ему символ Em. Последующие наблюдения Резерфорда в 1901 году показали, что и препараты радия также испускают некую эманацию, которая обладает радиоактивными свойствами и ведёт себя как инертный газ[5], однако он в этой работе отметил приоритет супругов Кюри в открытии эманации. В 1903 году французский химик Андре-Луи Дебьерн обнаружил короткоживущую эманацию актиния[6].
Первоначально эманацию тория называли торо́ном, эманацию радия — радо́ном, актиния — актино́ном. Было доказано, что все эманации на самом деле представляют собой радионуклиды нового элемента — инертного газа, которому отвечает атомный номер 86. Впервые его выделили в чистом виде и измерили его плотность Уильям Рамзай и Роберт Уитлоу-Грей в 1908 году[7], они же предложили назвать газ нитон (от лат. nitens, светящийся). В 1923 году газ получил окончательное название радон, и символ Em был сменён на Rn.
В публичной лекции 1936 года Резерфорд кратко изложил итоги их работ:
Я помогал ему [профессору по электротехнике Оуэнсу в университете МакГилл в г. Монреале в Канаде с декабря 1898 года по 26 мая 1899 года] в проведении экспериментов, и мы обнаружили некоторые очень странные явления. Оказалось, что радиоактивное воздействие окиси тория может проходить сквозь дюжину листков бумаги, положенных поверх этой окиси, но задерживается тончайшей пластинкой слюды, как будто излучается что-то, способное диффундировать сквозь поры бумаги. Тот факт, что прибор был очень чувствителен к движению воздуха, поддерживал эту диффузионную гипотезу. Затем мы провели эксперименты, в которых воздух проходил над окисью тория, а потом попадал в ионизационную камеру. Эти опыты показали, что активность может переноситься воздухом. Однако, когда поток воздуха прекращался, активность в ионизационной камере не сразу исчезала, а уменьшалась постепенно по экспоненциальному закону. Я назвал это газообразное вещество, которое может диффундировать сквозь бумагу, переноситься воздухом и в течение некоторого времени сохранять свою активность, исчезающую по характерному закону, «эманацией тория».
Я установил, что эта эманация обладает чрезвычайно своеобразным свойством делать радиоактивными тела, над которыми она проходит. Казалось, что это свойство, скорее всего, обусловлено осаждением некой материальной субстанции, а не какой-либо активностью, возникшей в самих телах под действием излучения, так как тогда количество осаждённого вещества должно увеличиваться при приложении электрического поля. В те времена многие получали неповторяющиеся и странные результаты, помещая предметы вблизи радиоактивных веществ. По-видимому, всё это могло объясняться наличием таких же эманаций, как обнаруженная нами у тория.
Прежде чем считать такое объяснение правильным, необходимо было выяснить истинную природу эманации. Это было очень трудно, так как доступное количество её всегда было очень мало.
Заслуга открытия радона как химического элемента часто приписывается также немецкому химику Фридриху Дорну. Вопросы приоритета в открытии радона рассматриваются в работе Джеймса и Вирджинии Маршалл[8], где показано, что первооткрывателем радона как химического элемента следует считать Резерфорда.
В 1900 году Дорн открыл изотоп радона 222Rn с периодом полураспада 3,823 дня и опубликовал статью[9][10] об этом, сославшись на более раннюю работу Резерфорда. Резерфорд, сперва с Оуэнсом, а затем один в 1899 году работал с другим изотопом 220Rn (тороном), период полураспада которого около 55,6 секунды. Резерфорд не знал о работах немца, так как тот опубликовал свою работу в немецком журнале с небольшим тиражом. Резерфорд не знал немецкого. Дорн совершенно не интересовался радиоактивностью. И только в 1902 году Резерфорд и Содди экспериментально доказали, что эманация — это изотоп радона. Они сумели её охладить и превратить в жидкость с помощью новой физической установки в университете МакГилл и опубликовали статьи.
Видео по теме
Нахождение в природе

Входит в состав радиоактивных рядов 238U, 235U и 232Th. Ядра радона постоянно возникают в природе при радиоактивном распаде материнских ядер. Равновесное содержание в земной коре 7·10–16% по массе. Ввиду химической инертности радон относительно легко покидает кристаллическую решётку «родительского» минерала и попадает в подземные воды, природные газы и воздух. Поскольку наиболее долгоживущим из четырёх природных изотопов радона (218, 219, 220, 222) является 222Rn, именно его содержание в этих средах максимально.
Концентрация радона в воздухе зависит, в первую очередь, от геологической обстановки (так, граниты, в которых много урана, являются активными источниками радона, в то же время над поверхностью морей радона мало), а также от погоды (во время дождя микротрещины, по которым радон поступает из почвы, заполняются водой; снежный покров также препятствует доступу радона в воздух).
Перед землетрясениями наблюдается повышение концентрации радона в воздухе, благодаря сейсмической активности[11]. Выход радона из земли в это время называется эксхаляция[12]
Получение
Для получения радона через водный раствор любой соли радия-226 продувают воздух, который уносит с собой радон-222, образующийся при радиоактивном распаде радия-226. Далее воздух тщательно фильтруют для отделения микрокапель раствора, содержащего соль радия, которые могут быть захвачены током воздуха. Для получения собственно радона из смеси газов удаляют химически активные вещества (кислород, водород, водяные пары и т. д.), остаток конденсируют жидким азотом, затем из конденсата отгоняют азот и инертные газы (аргон, неон и т. д.).
В одном грамме радия-226 возникает за сутки около 1 мм3 радона-222.
Физические свойства
 Эмиссионный спектр радона, сфотографированный Э. Резерфордом в 1908 году. Числа на краях спектра представляют собой длины волн. Средний спектр принадлежит радону, внешние спектры — гелию (добавлены для калибровки длин волн)
Эмиссионный спектр радона, сфотографированный Э. Резерфордом в 1908 году. Числа на краях спектра представляют собой длины волн. Средний спектр принадлежит радону, внешние спектры — гелию (добавлены для калибровки длин волн)Радон — радиоактивный одноатомный тяжёлый газ без цвета и запаха. Растворимость в воде при комнатной температуре составляет 460 мл/л, что выше, чем растворимость более лёгких инертных газов. В органических растворителях и в жировой ткани человека растворимость радона в десятки раз выше, чем в воде. Газ хорошо просачивается сквозь полимерные плёнки. Легко адсорбируется активированным углём и силикагелем.
Собственная радиоактивность радона вызывает его флюоресценцию. Газообразный и жидкий радон флюоресцирует голубым светом, у твёрдого радона при охлаждении до азотных температур цвет флюоресценции становится сперва жёлтым, затем — красно-оранжевым.
Цвет свечения в газовом разряде у радона — синий, так как в видимой части спектра радона особо выделяются 8 линий, отвечающих длинам волн от 3982 до 5085 Å и лежащих главным образом в синей части спектра[13], однако из-за отсутствия стабильных изотопов применение его в газосветных приборах невозможно.
Плотность радона при нормальных условиях составляет 9,73 кг/м3, что примерно в 7,6 раз больше плотности воздуха.
Химические свойства
 схема электронных оболочек радона
схема электронных оболочек радонаВ химическом отношении радон является наиболее активным из благородных газов, так как его электроны внешних электронных оболочек имеют относительную низкую энергию ионизации.
Радон образует химические соединения с фтором. Так, дифторид радона RnF2 является белым нелетучим кристаллическим веществом.
Фториды радона могут быть получены также под действием сильных фторирующих агентов (например, фторидов галогенов: ClF3, BrF5, IF7[14]).
Получены также соединения с катионом RnF+: RnF[SbF6], RnF[Sb2F11][14].
Кроме фтора, радон может образовывать бинарные соединения с кислородом; в частности, был получен триоксид радона[15], однако получение других оксидов радона не подтверждено.
Кроме того, радон может входить в состав различных клатратов, которые, хотя и имеют постоянный стехиометрический состав, не образуют химических связей с участием атомов радона.
Применение
Радон используют в медицине для приготовления радоновых ванн (при этом их эффективность научно не доказана[источник не указан 499 дней]). Радон используется в сельском хозяйстве для активации кормов домашних животных[1], в металлургии в качестве индикатора при определении скорости газовых потоков в доменных печах, газопроводах. В геологии измерение содержания радона в воздухе и воде применяется для поиска месторождений урана и тория, а также активных тектонических разломов, на наличие которых может указывать повышенное содержание радона в приземном и подпочвенном воздухе; в гидрогеологии — для исследования взаимодействия грунтовых и речных вод.
Динамика концентрации радона в подземных водах может применяться для прогноза землетрясений[16].
История
Открытие радиоактивности и радона совпало с повышением интереса к биологическим эффектам радиации. Было установлено, что вода многих источников минеральных вод богата эманацией радия (так именовался радон в то время). Вслед за этим открытием последовала волна моды «на радиацию». В частности, в рекламе того времени радиоактивность минеральных вод выдавалась за главный показатель их полезности и эффективности.
Радиационный фон помещений
Радиационный фон помещений зданий (РФП) — излучение земного и космического происхождения постоянно воздействующее на человека при его нахождении в пространстве внутри здания. РФП формируется, как естественный и технологически измененный радиационный фон; обычно причиной возникновения радиационного фона в зданиях является активность трех основных естественных долгоживущих радионуклидов: радий-226, торий-232 и калий-40, а также техногенного цезия-137 в строительных материалах и активность в воздухе короткоживущих изотопов (Т1/2<10 сут) радия и крайне редко тория. Основные составляющие радиационного фона помещений в значительной степени зависят от деятельности человека. Это вызвано, прежде всего, такими факторами, как выбор площадки для строительства, радиационных характеристик строительных материалов, конструктивных решений зданий и применяемых в них систем вентиляции[17][18]. Измерения не всегда подтверждают сложившийся вывод о том, что в подвальных помещениях и на нижних этажах зданий радон скапливается в больших концентрациях, чем на верхних. Безопасной средней по площади здания плотность потока радона на поверхности грунта считается менее 80 мБк/м2с для жилых зданий и 40 мБк/м2с для малоэтажных коттеджей[19].
Биологическое воздействие
Радон радиотоксичен и канцерогенен. Попадая в организм человека, он способствует процессам, приводящим к раку лёгкого. Распад ядер радона и его дочерних изотопов в лёгочной ткани вызывает микроожог, поскольку вся энергия альфа-частиц поглощается практически в точке распада. Особенно опасно (повышает риск заболевания) сочетание воздействия радона и курения. По данным департамента здравоохранения США радон — второй по частоте (после курения) фактор, вызывающий рак лёгких преимущественно бронхогенного (центрального) типа. Рак лёгких, вызванный радоновым облучением, является шестой по частоте причиной смерти от рака[20].
Радон и его дочерние продукты обусловливают более половины всей эффективной дозы облучения, которую в среднем получает организм человека от природных и техногенных радионуклидов окружающей среды.
В настоящее время во многих странах проведен мониторинг концентрации радона в зданиях как первый этап оптимизации защиты населения[21].
МКРЗ установила референтный уровень объемной активности радона в жилище на уровне 300 Бк/куб.м.[22]
Тестирование и снижение уровня радона
 | Этот раздел описывает ситуацию применительно лишь к одному региону, возможно, нарушая при этом правило о взвешенности изложения. Вы можете помочь Википедии, добавив информацию для других стран и регионов. |
 Цифровой измеритель уровня радона
Цифровой измеритель уровня радонаСуществуют достаточно простые тесты, позволяющие измерить уровень радона. В некоторых странах такие тесты методически проводятся в местах, где систематически наблюдаются угрозы. Устройства для измерения уровня радона имеются в продаже. Цифровые устройства для измерения радона позволяют проводить текущие измерения, производящие ежедневные, еженедельные, краткосрочные и долгосрочные отчеты с помощью цифрового дисплея. Устройства для краткосрочного первоначального тестирования уровня радона недороги, и в некоторых случаях бесплатны. Существуют строгие правила проведения краткосрочных тестов, и их соблюдение крайне важно. Комплект для измерения уровня радона включает в себя коллектор, который необходимо повесить на нижнем этаже жилого дома на период от 2х до 7 дней. Далее пользователю необходимо отправить коллектор в лабораторию для анализа. Также доступны приборы для долгосрочного (на срок до одного года) измерения уровня радона. Есть возможность измерения количества выделяемого из земли радона до начала строительства [23]. Концентрация радона может меняться ежедневно, поэтому необходимы долгосрочные измерения средней концентрации радона в помещениях, где человек проводит значительную часть времени [24].
Концентрация радона подвержена естественным колебаниям из-за таких факторов, как смена погодных условий, поэтому первоначальный тест может дать неточный результат относительно средней концентрации радона. Уровень радона в воздухе максимален в наиболее холодной части дня, когда перепады давления наиболее велики[25]. Поэтому при обнаружении высокой концентрации радона (более 4 pCi/L) оправдано проведение повторных измерений перед осуществлением более дорогостоящих мероприятий по борьбе с выделением газа. Показания в промежутке от 4 до 10 pCi/L являются показанием к проведению долгосрочного теста. Показания выше 10 pCi/L требуют только дополнительного краткосрочного теста, дабы избежать чрезмерного промедления в борьбе с выделением газа. Покупателям недвижимости рекомендуется отложить или отказаться от покупки, если продавец не смог снизить уровень радона до 4 pCi/L или менее[23].
Поскольку период полураспада радона составляет всего 3,8 дней, удаление или изоляция источника значительно снижает угрозу в течение нескольких недель. Также можно снизить концентрацию радона с помощью изменения вентилирования сооружения. Концентрация радона, как правило, снижается при вентиляции помещения[26]. В хорошо проветриваемых помещениях концентрация радона имеет тенденцию выравниваться до уровня улицы (обычно 10 Бк/м3, в пределах от 1 до 100 Бк/м3)[23].
Есть четыре основных способа снизить концентрацию радона в домах[23][27]:
- Разгерметизация (всасывание почвы) за счет увеличения вентилирования между этажами
- Улучшение вентиляции помещения и предотвращение проникновения радона из подвальных помещений в жилые помещения
- Установка системы для удаления радона из подвальных помещений
- Установка систем вентиляции с положительным давлением
Согласно EPA[23], для уменьшения концентрации радона в первую очередь используются система труб дефлектора и вентилятор, высасывающие радон из-под дома наружу. Концентрация радона в помещении, как правило, может быть уменьшена с помощью разгерметизации и перенаправления загрязненного радоном воздуха в открытое пространство, вдалеке от окон и строительных отверстий. EPA рекомендует использовать методы, препятствующие проникновения радона в помещение. Всасывание почвы, например, предотвращает появление радона в доме, потому что радон из-под дома выпускается наружу через трубы, где он разбавляется[28]. EPA не рекомендует использовать герметизацию без других мер, поскольку использование такого метода не приводит к значительным и последовательным снижениям уровня радона[28].
Система вентиляции с положительным давлением может быть объединена с теплообменником для восстановления энергии в процессе воздухообмена с воздухом извне, поскольку исключительно выведение воздуха наружу может быть недостаточным решением, так как это может привести к всасыванию воздуха в жилище. В дома, построенные над погребами, можно установить листы пластика, покрывающие пустое пространство — это будет барьером для радона [23]. Вентиляционная труба и вентилятор используются для выведения радона из-под пласта пластика на открытый воздух. Этот способ выведения радона называется «подмембранное всасывание», и при правильном применении оно является самым эффективным способом выведения радона в домах с погребным помещением[24].
Изотопы
Радон не имеет стабильных изотопов. Наиболее устойчив 222Rn (T1/2=3,8235 суток), входящий в природное радиоактивное семейство урана-238 (семейство урана-радия) и являющийся непосредственным продуктом распада радия-226. Иногда название «радон» относят именно к этому изотопу. В семейство тория-232 входит 220Rn (T1/2=55,6 с), иногда его называют торон (Tn). В семейство урана-235 (урана-актиния) входит 219Rn (T1/2=3,96 с), его называют актинон (An). В одну из побочных ветвей (коэффициент ветвления 2·10−7) семейства урана-радия входит также очень короткоживущий (T1/2=35 мс) радон-218. Все отмеченные изотопы радона испытывают альфа-распад. Этими четырьмя нуклидами исчерпывается список природных изотопов радона. Известны ещё 30 искусственных изотопов Rn с массовым числом от 195 до 228. Некоторые нейтронодефицитные изотопы радона имеют также возбуждённые метастабильные состояния; таких состояний известно 13. Преобладающие моды распада у лёгких изотопов Rn — альфа-распад, позитронный распад и электронный захват. Начиная с массового числа A=212 альфа-распад становится доминирующим. Тяжёлые изотопы радона (начиная с A=223) распадаются преимущественно посредством бета-минус-распада.
Примечания
- ↑ 1 2 3 Химическая энциклопедия / Редкол.: Кнунянц И. Л. и др.. — М.: Советская энциклопедия, 1995. — Т. 4 (Пол-Три). — 639 с. — ISBN 5-82270-092-4.
- ↑ P.Curie, Mme. Marie Curie (1899). «Sur la radioactivite provoquee par les rayons de Becquerel». Comptes rendus hebdomadaires des séances de l’Académie des sciences 129: 714–716.
- ↑ E. Rutherford, R. B. Owens (1899). «Thorium and uranium radiation». Trans. R. Soc. Can. 2: 9–12.
- ↑ Rutherford, E. (1900). «A radioactive substance emitted from thorium compounds». Phil. Mag. 40: 1–4.
- ↑ E. Rutherford, H.T. Brooks (1901). «The new gas from radium». Trans. R. Soc. Can. 7: 21–25.
- ↑ Debierne, André-Louis (1903). «Sur la radioactivite induite provoquee par les sels d’actinium». Comptes rendus hebdomadaires des seances de l’Academie des sciences 136.
- ↑ W.Ramsay, R. W. Gray (1910). «La densité de l’emanation du radium». Comptes rendus hebdomadaires des seances de l’Academie des sciences 151: 126–128.
- ↑ James L. Marshall and Virginia R. Marshall (2003). «ERNEST RUTHERFORD, THE «TRUE DISCOVERER» OF RADON». Bulletin for the History of Chemistry 28 (2): 76-83.
- ↑ Dorn, Friedrich Ernst (1900). «Ueber die von radioaktiven Substanzen ausgesandte Emanation». Abhandlungen der Naturforschenden Gesellschaft zu Halle 22.
- ↑ Dorn, F. E. (1900). «Die von radioactiven Substanzen ausgesandte Emanation». Abhandlungen der Naturforschenden Gesellschaft zu Halle 23: 1–15.
- ↑ Уткин В. И., Юрков А. К. Радон как «детерминированный» индикатор природных и техногенных геодинамических процессов // Доклады РАН. 2009. Т. 426. № 6. С. 816—820.
- ↑ Уткин В. И., Юрков А. К. Отражение сейсмических событий в поле эксхаляции радона // Геофизика. 1997. № 6. С. 50-56.
- ↑ Михайленко Я. И. Курс общей и неорганической химии. — 1966. — С. 635. — 664 с.
- ↑ 1 2 Леонтьев А. В., Фомичева О. А., Проскурнина М. В., Зефиров Н. С. (1982). «Современное состояние химии радона». Успехи химии 51 (1): 23-39.
- ↑ A. G. Sykes. Recent Advances in Noble-Gas Chemistry // Advances in Inorganic Chemistry. — Academic Press, 1998. — Vol. 46. — P. 91–93. — ISBN 978-0120236466.
- ↑ Уткин В. И., Юрков А. К. Динамика выделения радона из массива горных пород как краткосрочный предвестник землетрясения // Докл. РАН. 1998. Т. 358. № 5. С. 675-680.
- ↑ Крисюк, Э.М. Радиационный фон помещений. — М.: Энергоатомиздат, 1989. — 120 с. — ISBN 5-283-02992-1.
- ↑ Р. А. Назиров, Е.В. Пересыпкин, И.В. Тарасов, В.И. Верещагин. Снижение естественной радиоактивности цементных бетонов // Известия высших учебных заведений. Строительство : науч. — теоретич. журн./ М-во высш. и сред. специального образования РФ, Ассоц. строит. вузов СНГ, Новосиб. гос. архитектурно — строит. ун-т. : журнал. — 2007. — Январь (№ 1). — С. 45—49. — ISSN 0536-1052.
- ↑ Таблица № 2 ТСН РБ-2003 МО
- ↑ S. Darby, D. Hill, R. Doll (2001). «Radon: A likely carcinogen at all exposures». Annals of Oncology 12 (10): 27. DOI:10.1023/A:1012518223463.
- ↑ WHO Handbook on Indoor Radon: A Public Health Perspective. — Geneva: World Health Organization, 2009-01-01. — (WHO Guidelines Approved by the Guidelines Review Committee). — ISBN 9789241547673.
- ↑ M. Tirmarche, J. D. Harrison, D. Laurier, F. Paquet, E. Blanchardon. ICRP Publication 115. Lung cancer risk from radon and progeny and statement on radon // Annals of the ICRP. — 2010-02-01. — Т. 40, вып. 1. — С. 1–64. — ISSN 1872-969X. — DOI:10.1016/j.icrp.2011.08.011.
- ↑ 1 2 3 4 5 6 United States Environmental Protection Agency. «A Citizen’s Guide to Radon».
- ↑ 1 2 Baes, Fred. Environmental and Background Radiation — Radon.
- ↑ Thad. Godish, (2001) . «Indoor Environment Quality». Boca Raton, FL. CRC Press LLC.
- ↑ Agency for Toxic Substances and Disease Registry, U.S. Public Health Service, In collaboration with U.S. Environmental Protection Agency. Toxicological profile for radon.
- ↑ World Health Organization. Radon and cancer, fact sheet 291.
- ↑ 1 2 Consumer’s Guide to Radon Reduction: How to fix your home.
Ссылки
Радон Википедия
| Радон | |
|---|---|
| ← Астат | Франций → | |
| Бесцветный, слегка флюоресцирующий радиоактивный газ | |
| Название, символ, номер | Радо́н / Radon (Rn), 86 |
| Атомная масса (молярная масса) | 222,0176 (наиболее стабильный изотоп) а. е. м. (г/моль) |
| Электронная конфигурация | [Xe] 4f14 5d10 6s2 6p6 |
| Радиус атома | 214 пм |
| Ковалентный радиус | 140—150 пм |
| Степени окисления | +2, +4, +6, +8[1] |
| Энергия ионизации (первый электрон) | 1036,5 (10,74) кДж/моль (эВ) |
| Плотность (при н. у.) | (газ, при 0 °C) 9,81 кг/м3 (жидк., при −62 °C) 4,4 г/см³ |
| Температура плавления | 202 K (−71,15 °C) |
| Температура кипения | 211,4 K (−61,75 °C) |
| Уд. теплота плавления | 2,7 кДж/моль |
| Уд. теплота испарения | 18,1 кДж/моль |
| Молярная теплоёмкость | 20,79[1] Дж/(K·моль) |
| Структура решётки | кубическая гранецентрированая |
| Теплопроводность | (300 K) (газ, при 0 °C) 0,0036 Вт/(м·К) |
| Номер CAS | 10043-92-2 |
| 86 | Радон |
| 4f145d106s26p6 | |
Радо́н — элемент 18-й группы периодической системы химических элементов Д. И. Менделеева (по старой классификации — главной подгруппы 8-й группы), 6-го периода, с атомным номером 86. Обозначается символом Rn (лат. Radon). Простое вещество радон при нормальных условиях — бесцветный инертный газ; радиоактивен, стабильных изотопов не имеет, может представлять опасность для здоровья и жизни. При комнатной температуре является одним из самых тяжёлых газов. Наиболее стабильный изотоп (222Rn) имеет период полураспада 3,8 суток.
История открытия и происхождение названия
В 1899 году Пьер и Мария Кюри обнаружили, что газ, находившийся в контакте с радием, остаётся радиоактивным в течение месяца[2]. Эрнест Резерфорд и Роберт Оуэнс позже в том же году отметили[3], что радиоактивность препаратов тория колеблется со временем. Позже Резерфорд объяснил это тем, что торий испускает, кроме α-частиц, и некое неизвестное ранее вещество, так что воздух вокруг препаратов тория постепенно становится радиоактивным[4]. Это вещество он предложил назвать эмана́цией (от лат. emanatio «истечение») тория и дать ему символ Em. Последующие наблюдения Резерфорда в 1901 году показали, что и препараты радия также испускают некую эманацию, которая обладает радиоактивными свойствами и ведёт себя как инертный газ[5], однако он в этой работе отметил приоритет супругов Кюри в открытии эманации. В 1903 году французский химик Андре-Луи Дебьерн обнаружил короткоживущую эманацию актиния[6].
Первоначально эманацию тория называли торо́ном, эманацию радия — радо́ном, актиния — актино́ном. Было доказано, что все эманации на самом деле представляют собой радионуклиды нового элемента — инертного газа, которому отвечает атомный номер 86. Впервые его выделили в чистом виде и измерили его плотность Уильям Рамзай и Роберт Уитлоу-Грей в 1908 году[7], они же предложили назвать газ нитон (от лат. nitens, светящийся). В 1923 году газ получил окончательное название радон, и символ Em был сменён на Rn.
В публичной лекции 1936 года Резерфорд кратко изложил итоги их работ:
Я помогал ему [профессору по электротехнике Оуэнсу в университете МакГилл в г. Монреале в Канаде с декабря 1898 года по 26 мая 1899 года] в проведении экспериментов, и мы обнаружили некоторые очень странные явления. Оказалось, что радиоактивное воздействие окиси тория может проходить сквозь дюжину листков бумаги, положенных поверх этой окиси, но задерживается тончайшей пластинкой слюды, как будто излучается что-то, способное диффундировать сквозь поры бумаги. Тот факт, что прибор был очень чувствителен к движению воздуха, поддерживал эту диффузионную гипотезу. Затем мы провели эксперименты, в которых воздух проходил над окисью тория, а потом попадал в ионизационную камеру. Эти опыты показали, что активность может переноситься воздухом. Однако, когда поток воздуха прекращался, активность в ионизационной камере не сразу исчезала, а уменьшалась постепенно по экспоненциальному закону. Я назвал это газообразное вещество, которое может диффундировать сквозь бумагу, переноситься воздухом и в течение некоторого времени сохранять свою активность, исчезающую по характерному закону, «эманацией тория».
Я установил, что эта эманация обладает чрезвычайно своеобразным свойством делать радиоактивными тела, над которыми она проходит. Казалось, что это свойство, скорее всего, обусловлено осаждением некой материальной субстанции, а не какой-либо активностью, возникшей в самих телах под действием излучения, так как тогда количество осаждённого вещества должно увеличиваться при приложении электрического поля. В те времена многие получали неповторяющиеся и странные результаты, помещая предметы вблизи радиоактивных веществ. По-видимому, всё это могло объясняться наличием таких же эманаций, как обнаруженная нами у тория.
Прежде чем считать такое объяснение правильным, необходимо было выяснить истинную природу эманации. Это было очень трудно, так как доступное количество её всегда было очень мало.
Заслуга открытия радона как химического элемента часто приписывается также немецкому химику Фридриху Дорну. Вопросы приоритета в открытии радона рассматриваются в работе Джеймса и Вирджинии Маршалл[8], где показано, что первооткрывателем радона как химического элемента следует считать Резерфорда.
В 1900 году Дорн открыл изотоп радона 222Rn с периодом полураспада 3,823 дня и опубликовал статью[9][10] об этом, сославшись на более раннюю работу Резерфорда. Резерфорд, сперва с Оуэнсом, а затем один в 1899 году работал с другим изотопом 220Rn (тороном), период полураспада которого около 55,6 секунды. Резерфорд не знал о работах немца, так как тот опубликовал свою работу в немецком журнале с небольшим тиражом. Резерфорд не знал немецкого. Дорн совершенно не интересовался радиоактивностью. И только в 1902 году Резерфорд и Содди экспериментально доказали, что эманация — это изотоп радона. Они сумели её охладить и превратить в жидкость с помощью новой физической установки в университете МакГилл и опубликовали статьи.
Нахождение в природе
Входит в состав радиоактивных рядов 238U, 235U и 232Th. Ядра радона постоянно возникают в природе при радиоактивном распаде материнских ядер. Равновесное содержание в земной коре 7⋅10–16% по массе. Ввиду химической инертности радон относительно легко покидает кристаллическую решётку «родительского» минерала и попадает в подземные воды, природные газы и воздух. Поскольку наиболее долгоживущим из четырёх природных изотопов радона (218, 219, 220, 222) является 222Rn, именно его содержание в этих средах максимально.
Концентрация радона в воздухе зависит, в первую очередь, от геологической обстановки (так, граниты, в которых много урана, являются активными источниками радона, в то же время над поверхностью морей радона мало), а также от погоды (во время дождя микротрещины, по которым радон поступает из почвы, заполняются водой; снежный покров также препятствует доступу радона в воздух).
Перед землетрясениями наблюдается повышение концентрации радона в воздухе, благодаря сейсмической активности[11]. Выход радона из земли в это время называется эксхаляцией[12]
Получение
Для получения радона через водный раствор любой соли радия-226 продувают воздух, который уносит с собой радон-222, образующийся при радиоактивном распаде радия-226. Далее воздух тщательно фильтруют для отделения микрокапель раствора, содержащего соль радия, которые могут быть захвачены током воздуха. Для получения собственно радона из смеси газов удаляют химически активные вещества (кислород, водород, водяные пары и т. д.), остаток конденсируют жидким азотом, затем из конденсата отгоняют азот и инертные газы (аргон, неон и т. д.).
В одном грамме радия-226 возникает за сутки около 0,1 мм3[13] радона-222.
Физические свойства
Эмиссионный спектр радона, сфотографированный Э. Резерфордом в 1908 году. Числа на краях спектра представляют собой длины волн. Средний спектр принадлежит радону, внешние спектры — гелию (добавлены для калибровки длин волн)Радон — радиоактивный одноатомный тяжёлый газ без цвета и запаха. Растворимость в воде при комнатной температуре составляет 460 мл/л, что выше, чем растворимость более лёгких инертных газов. В органических растворителях и в жировой ткани человека растворимость радона в десятки раз выше, чем в воде. Газ хорошо просачивается сквозь полимерные плёнки. Легко адсорбируется активированным углём и силикагелем.
Собственная радиоактивность радона вызывает его флюоресценцию. Газообразный и жидкий радон флюоресцирует голубым светом, у твёрдого радона при охлаждении до азотных температур цвет флюоресценции становится сперва жёлтым, затем — красно-оранжевым.
Цвет свечения в газовом разряде у радона — синий, так как в видимой части спектра радона особо выделяются 8 линий, отвечающих длинам волн от 3982 до 5085 Å (от 398,2 нм до 508,5 нм) и лежащих главным образом в синей части спектра[14], однако из-за отсутствия стабильных изотопов применение его в газосветных приборах невозможно.
Плотность радона при нормальных условиях составляет 9,73 кг/м3, что примерно в 7,6 раз больше плотности воздуха.
Химические свойства
схема электронных оболочек радонаВ химическом отношении радон является наиболее активным из благородных газов, так как его электроны внешних электронных оболочек имеют относительную низкую энергию ионизации.
Радон образует химические соединения с фтором. Так, дифторид радона RnF2 является белым нелетучим кристаллическим веществом.
Фториды радона могут быть получены также под действием сильных фторирующих агентов (например, фторидов галогенов: ClF3, BrF5, IF7[15]).
Получены также соединения с катионом RnF+: RnF[SbF6], RnF[Sb2F11][15].
Кроме фтора, радон может образовывать бинарные соединения с кислородом; в частности, был получен триоксид радона[16], однако получение других оксидов радона не подтверждено.
Кроме того, радон может входить в состав различных клатратов, которые, хотя и имеют постоянный стехиометрический состав, не образуют химических связей с участием атомов радона.
Применение
Радон используют в медицине для приготовления радоновых ванн. Радон используется в сельском хозяйстве для активации кормов домашних животных[1], в металлургии в качестве индикатора при определении скорости газовых потоков в доменных печах, газопроводах. В геологии измерение содержания радона в воздухе и воде применяется для поиска месторождений урана и тория, а также активных тектонических разломов, на наличие которых может указывать повышенное содержание радона в приземном и подпочвенном воздухе; в гидрогеологии — для исследования взаимодействия грунтовых и речных вод.
Динамика концентрации радона в подземных водах может применяться для прогноза землетрясений[17].
История
Открытие радиоактивности и радона совпало с повышением интереса к биологическим эффектам радиации. Было установлено, что вода многих источников минеральных вод богата эманацией радия (так именовался радон в то время). Вслед за этим открытием последовала волна моды «на радиацию». В частности, в рекламе того времени радиоактивность минеральных вод выдавалась за главный показатель их полезности и эффективности.
Радиационный фон помещений
Радиационный фон помещений зданий (РФП) — излучение земного и космического происхождения, постоянно воздействующее на человека при его нахождении в пространстве внутри здания. РФП формируется, как естественный и технологически измененный радиационный фон; обычно причиной возникновения радиационного фона в зданиях является активность трех основных естественных долгоживущих радионуклидов: радий-226, торий-232 и калий-40, а также техногенного цезия-137 в строительных материалах и активность в воздухе короткоживущих изотопов (Т1/2<10 сут) радия и крайне редко тория. Основные составляющие радиационного фона помещений в значительной степени зависят от деятельности человека. Это вызвано, прежде всего, такими факторами, как выбор площадки для строительства, радиационных характеристик строительных материалов, конструктивных решений зданий и применяемых в них систем вентиляции[18][19]. Измерения не всегда подтверждают сложившийся вывод о том, что в подвальных помещениях и на нижних этажах зданий радон скапливается в больших концентрациях, чем на верхних. Безопасной средней по площади здания плотность потока радона на поверхности грунта считается менее 80 мБк/м2с для жилых зданий и 40 мБк/м2с для малоэтажных коттеджей[20].
Биологическое воздействие
Радон радиотоксичен и канцерогенен. Попадая в организм человека, он способствует процессам, приводящим к раку лёгкого. Распад ядер радона и его дочерних изотопов в лёгочной ткани вызывает микроожог, поскольку вся энергия альфа-частиц поглощается практически в точке распада. Особенно опасно (повышает риск заболевания) сочетание воздействия радона и курения. По данным департамента здравоохранения США радон — второй по частоте (после курения) фактор, вызывающий рак лёгких преимущественно бронхогенного (центрального) типа. Рак лёгких, вызванный радоновым облучением, является шестой по частоте причиной смерти от рака[21].
Радон и его дочерние продукты обусловливают более половины всей эффективной дозы облучения, которую в среднем получает организм человека от природных и техногенных радионуклидов окружающей среды.
В настоящее время во многих странах проведен мониторинг концентрации радона в зданиях как первый этап оптимизации защиты населения[22].
МКРЗ установила референтный уровень объемной активности радона в жилище на уровне 300 Бк/куб.м.[23]
Тестирование и снижение уровня радона
| Этот раздел описывает ситуацию применительно лишь к одному региону, возможно, нарушая при этом правило о взвешенности изложения. Вы можете помочь Википедии, добавив информацию для других стран и регионов. |
Существуют достаточно простые тесты, позволяющие измерить уровень радона. В некоторых странах такие тесты методически проводятся в местах, где систематически наблюдаются угрозы. Устройства для измерения уровня радона имеются в продаже. Цифровые устройства для измерения радона позволяют проводить текущие измерения, производящие ежедневные, еженедельные, краткосрочные и долгосрочные отчеты с помощью цифрового дисплея. Устройства для краткосрочного первоначального тестирования уровня радона недороги, и в некоторых случаях бесплатны. Существуют строгие правила проведения краткосрочных тестов, и их соблюдение крайне важно. Комплект для измерения уровня радона включает в себя коллектор, который необходимо повесить на нижнем этаже жилого дома на период от 2х до 7 дней. Далее пользователю необходимо отправить коллектор в лабораторию для анализа. Также доступны приборы для долгосрочного (на срок до одного года) измерения уровня радона. Есть возможность измерения количества выделяемого из земли радона до начала строительства [24]. Концентрация радона может меняться ежедневно, поэтому необходимы долгосрочные измерения средней концентрации радона в помещениях, где человек проводит значительную часть времени [25].
Концентрация радона подвержена естественным колебаниям из-за таких факторов, как смена погодных условий, поэтому первоначальный тест может дать неточный результат относительно средней концентрации радона. Уровень радона в воздухе максимален в наиболее холодной части дня, когда перепады давления наиболее велики[26]. Поэтому при обнаружении высокой концентрации радона (более 4 pCi/L) оправдано проведение повторных измерений перед осуществлением более дорогостоящих мероприятий по борьбе с выделением газа. Показания в промежутке от 4 до 10 pCi/L являются показанием к проведению долгосрочного теста. Показания выше 10 pCi/L требуют только дополнительного краткосрочного теста, дабы избежать чрезмерного промедления в борьбе с выделением газа. Покупателям недвижимости рекомендуется отложить или отказаться от покупки, если продавец не смог снизить уровень радона до 4 pCi/L или менее[24].
Поскольку период полураспада радона составляет всего 3,8 дней, удаление или изоляция источника значительно снижает угрозу в течение нескольких недель. Также можно снизить концентрацию радона с помощью изменения вентилирования сооружения. Концентрация радона, как правило, снижается при вентиляции помещения[27]. В хорошо проветриваемых помещениях концентрация радона имеет тенденцию выравниваться до уровня улицы (обычно 10 Бк/м3, в пределах от 1 до 100 Бк/м3)[24].
Есть четыре основных способа снизить концентрацию радона в домах[24][28]:
- Разгерметизация (всасывание почвы) за счет увеличения вентилирования между этажами
- Улучшение вентиляции помещения и предотвращение проникновения радона из подвальных помещений в жилые помещения
- Установка системы для удаления радона из подвальных помещений
- Установка систем вентиляции с положительным давлением
Согласно EPA[24], для уменьшения концентрации радона в первую очередь используются система труб дефлектора и вентилятор, высасывающие радон из-под дома наружу. Концентрация радона в помещении, как правило, может быть уменьшена с помощью разгерметизации и перенаправления загрязненного радоном воздуха в открытое пространство, вдалеке от окон и строительных отверстий. EPA рекомендует использовать методы, препятствующие проникновения радона в помещение. Всасывание почвы, например, предотвращает появление радона в доме, потому что радон из-под дома выпускается наружу через трубы, где он разбавляется[29]. EPA не рекомендует использовать герметизацию без других мер, поскольку использование такого метода не приводит к значительным и последовательным снижениям уровня радона[29].
Система вентиляции с положительным давлением может быть объединена с теплообменником для восстановления энергии в процессе воздухообмена с воздухом извне, поскольку исключительно выведение воздуха наружу может быть недостаточным решением, так как это может привести к всасыванию воздуха в жилище. В дома, построенные над погребами, можно установить листы пластика, покрывающие пустое пространство — это будет барьером для радона [24]. Вентиляционная труба и вентилятор используются для выведения радона из-под пласта пластика на открытый воздух. Этот способ выведения радона называется «подмембранное всасывание», и при правильном применении оно является самым эффективным способом выведения радона в домах с погребным помещением[25].
Изотопы
Радон не имеет стабильных изотопов. Наиболее устойчив 222Rn (T1/2=3,8235 суток), входящий в природное радиоактивное семейство урана-238 (семейство урана-радия) и являющийся непосредственным продуктом распада радия-226. Иногда название «радон» относят именно к этому изотопу. В семейство тория-232 входит 220Rn (T1/2=55,6 с), иногда его называют торон (Tn). В семейство урана-235 (урана-актиния) входит 219Rn (T1/2=3,96 с), его называют актинон (An). В одну из побочных ветвей (коэффициент ветвления 2⋅10−7) семейства урана-радия входит также очень короткоживущий (T1/2=35 мс) радон-218. Все отмеченные изотопы радона испытывают альфа-распад. Этими четырьмя нуклидами исчерпывается список природных изотопов радона. Известны ещё 30 искусственных изотопов Rn с массовым числом от 195 до 228. Некоторые нейтронодефицитные изотопы радона имеют также возбуждённые метастабильные состояния; таких состояний известно 13. Преобладающие моды распада у лёгких изотопов Rn — альфа-распад, позитронный распад и электронный захват. Начиная с массового числа A=212 альфа-распад становится доминирующим. Тяжёлые изотопы радона (начиная с A=223) распадаются преимущественно посредством бета-минус-распада.
Примечания
- ↑ 1 2 3 Химическая энциклопедия / Редкол.: Кнунянц И. Л. и др.. — М.: Советская энциклопедия, 1995. — Т. 4 (Пол-Три). — 639 с. — ISBN 5-82270-092-4.
- ↑ P.Curie, Mme. Marie Curie. Sur la radioactivite provoquee par les rayons de Becquerel (фр.) // Comptes rendus hebdomadaires des séances de l’Académie des sciences (англ.)русск. : magazine. — 1899. — Vol. 129. — P. 714—716.
- ↑ E. Rutherford, R. B. Owens. Thorium and uranium radiation (неопр.) // Trans. R. Soc. Can.. — 1899. — Т. 2. — С. 9—12.
- ↑ Rutherford, E. A radioactive substance emitted from thorium compounds (англ.) // Phil. Mag. : journal. — 1900. — Vol. 40. — P. 1—4.
- ↑ E. Rutherford, H.T. Brooks. The new gas from radium (неопр.) // Trans. R. Soc. Can.. — 1901. — Т. 7. — С. 21—25.
- ↑ Debierne, André-Louis. Sur la radioactivite induite provoquee par les sels d’actinium (фр.) // Comptes rendus hebdomadaires des seances de l’Academie des sciences (англ.)русск. : magazine. — 1903. — Vol. 136. — P. 446.
- ↑ W.Ramsay, R. W. Gray. La densité de l’emanation du radium (неопр.) // Comptes rendus hebdomadaires des seances de l’Academie des sciences (англ.)русск.. — 1910. — Т. 151. — С. 126—128.
- ↑ James L. Marshall and Virginia R. Marshall. ERNEST RUTHERFORD, THE «TRUE DISCOVERER» OF RADON (англ.) // Bulletin for the History of Chemistry (англ.)русск. : journal. — 2003. — Vol. 28, no. 2. — P. 76—83.
- ↑ Dorn, Friedrich Ernst. Ueber die von radioaktiven Substanzen ausgesandte Emanation (нем.) // Abhandlungen der Naturforschenden Gesellschaft zu Halle : magazin. — Stuttgart, 1900. — Bd. 22. — S. 155.
- ↑ Dorn, F. E. Die von radioactiven Substanzen ausgesandte Emanation (нем.) // Abhandlungen der Naturforschenden Gesellschaft zu Halle : magazin. — 1900. — Bd. 23. — S. 1—15.
- ↑ Уткин В. И., Юрков А. К. Радон как «детерминированный» индикатор природных и техногенных геодинамических процессов // Доклады РАН. 2009. Т. 426. № 6. С. 816—820.
- ↑ Уткин В. И., Юрков А. К. Отражение сейсмических событий в поле эксхаляции радона // Геофизика. 1997. № 6. С. 50-56.
- ↑ U.S. National Library of Medicine, National Center for Biotechnology Information. Ra-226, Other Experimental Properties (неопр.).
- ↑ Михайленко Я. И. Курс общей и неорганической химии. — 1966. — С. 635. — 664 с.
- ↑ 1 2 Леонтьев А. В., Фомичева О. А., Проскурнина М. В., Зефиров Н. С. Современное состояние химии радона (рус.) // Успехи химии. — Российская академия наук, 1982. — Т. 51, № 1. — С. 23—39.
- ↑ A. G. Sykes. Recent Advances in Noble-Gas Chemistry // Advances in Inorganic Chemistry (неопр.). — Academic Press, 1998. — Т. 46. — С. 91—93. — ISBN 978-0120236466.
- ↑ Уткин В. И., Юрков А. К. Динамика выделения радона из массива горных пород как краткосрочный предвестник землетрясения // Докл. РАН. 1998. Т. 358. № 5. С. 675-680.
- ↑ Крисюк, Э.М. Радиационный фон помещений. — М.: Энергоатомиздат, 1989. — 120 с. — ISBN 5-283-02992-1.
- ↑ Р. А. Назиров, Е.В. Пересыпкин, И.В. Тарасов, В.И. Верещагин. Снижение естественной радиоактивности цементных бетонов // Известия высших учебных заведений. Строительство : науч. — теоретич. журн./ М-во высш. и сред. специального образования РФ, Ассоц. строит. вузов СНГ, Новосиб. гос. архитектурно — строит. ун-т. : журнал. — 2007. — Январь (№ 1). — С. 45—49. — ISSN 0536-1052.
- ↑ Таблица № 2 ТСН РБ-2003 МО
- ↑ S. Darby, D. Hill, R. Doll. Radon: A likely carcinogen at all exposures (англ.) // Annals of Oncology (англ.)русск. : journal. — 2001. — Vol. 12, no. 10. — P. 27. — DOI:10.1023/A:1012518223463.
- ↑ WHO Handbook on Indoor Radon: A Public Health Perspective. — Geneva: World Health Organization, 2009-01-01. — (WHO Guidelines Approved by the Guidelines Review Committee). — ISBN 9789241547673.
- ↑ M. Tirmarche, J. D. Harrison, D. Laurier, F. Paquet, E. Blanchardon. ICRP Publication 115. Lung cancer risk from radon and progeny and statement on radon // Annals of the ICRP. — 2010-02-01. — Т. 40, вып. 1. — С. 1—64. — ISSN 1872-969X. — DOI:10.1016/j.icrp.2011.08.011.
- ↑ 1 2 3 4 5 6 United States Environmental Protection Agency. «A Citizen’s Guide to Radon» (неопр.).
- ↑ 1 2 Baes, Fred. Environmental and Background Radiation — Radon (неопр.).
- ↑ Thad. Godish, (2001) . «Indoor Environment Quality». Boca Raton, FL. CRC Press LLC.
- ↑ Agency for Toxic Substances and Disease Registry, U.S. Public Health Service, In collaboration with U.S. Environmental Protection Agency. Toxicological profile for radon (неопр.).
- ↑ World Health Organization. Radon and cancer, fact sheet 291 (неопр.).
- ↑ 1 2 Consumer’s Guide to Radon Reduction: How to fix your home (неопр.).
Ссылки
Радон, свойства атома, химические и физические свойства
Радон, свойства атома, химические и физические свойства.
Rn 86 Радон
222,0176*** 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 4f14 5s2 5p6 5d10 6s2 6p6
Радон — элемент периодической системы химических элементов Д. И. Менделеева с атомным номером 86. Расположен в 18-й группе (по старой классификации — главной подгруппе восьмой группы), шестом периоде периодической системы.
Общие сведения
Свойства атома
Химические свойства
Физические свойства
Таблица химических элементов Д.И. Менделеева
Общие сведения | |
| Название | Радон/ Radon |
| Символ | Rn |
| Номер в таблице | 86 |
| Тип | Неметалл |
| Открыт | Эрнест Резерфорд и Роберт Оуэнс, Англия, 1899 г. |
| Внешний вид и пр. | Бесцветный, слегка флюоресцирующий радиоактивный газ |
| Содержание в земной коре | |
| Содержание в океане | 6,0×10-20 % |
Свойства атома | |
| Атомная масса (молярная масса)*** | 222,0176 а. е. м. (г/моль) |
| Электронная конфигурация | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 4f14 5s2 5p6 5d10 6s2 6p6 |
| Радиус атома | 214 пм |
Химические свойства | |
| Степени окисления | +2, +4, +6, +8 |
| Валентность | 0 |
| Ковалентный радиус | 140-150 пм |
| Радиус иона | |
| Электроотрицательность | 2,2 (шкала Полинга) |
| Энергия ионизации (первый электрон) | 1036,5 кДж/моль (10,74 эВ) |
| Электродный потенциал | |
Физические свойства | |
| Плотность (при нормальных условиях) | 0,0098 г/см3 |
| Температура плавления | -71,15 °C (202 K) |
| Температура кипения | -61,75°C (211,4 K) |
| Уд. теплота плавления | 2,7 кДж/моль |
| Уд. теплота испарения | 18,1 кДж/моль |
| Молярная теплоёмкость | 20,79 Дж/(K·моль) |
| Молярный объём | |
| Теплопроводность (при 0 °C) | 0,0036 Вт/(м·К) |
| Электропроводность в твердой фазе | |
| Сверхпроводимость при температуре | |
| Твёрдость | 2,25 по шкале Мооса |
| Структура решётки | кубическая гранецентрированная |
| Параметры решётки | |
| Температура Дебая |
Примечание:
*** Указано значение атомной массы для стабильного изотопа.
Таблица химических элементов Д.И. Менделеева
- 1. Водород
- 2. Гелий
- 3. Литий
- 4. Бериллий
- 5. Бор
- 6. Углерод
- 7. Азот
- 8. Кислород
- 9. Фтор
- 10. Неон
- 11. Натрий
- 12. Магний
- 13. Алюминий
- 14. Кремний
- 15. Фосфор
- 16. Сера
- 17. Хлор
- 18. Аргон
- 19. Калий
- 20. Кальций
- 21. Скандий
- 22. Титан
- 23. Ванадий
- 24. Хром
- 25. Марганец
- 26. Железо
- 27. Кобальт
- 28. Никель
- 29. Медь
- 30. Цинк
- 31. Галлий
- 32. Германий
- 33. Мышьяк
- 34. Селен
- 35. Бром
- 36. Криптон
- 37. Рубидий
- 38. Стронций
- 39. Иттрий
- 40. Цирконий
- 41. Ниобий
- 42. Молибден
- 43. Технеций
- 44. Рутений
- 45. Родий
- 46. Палладий
- 47. Серебро
- 48. Кадмий
- 49. Индий
- 50. Олово
- 51. Сурьма
- 52. Теллур
- 53. Йод
- 54. Ксенон
- 55. Цезий
- 56. Барий
- 57. Лантан
- 58. Церий
- 59. Празеодим
- 60. Неодим
- 61. Прометий
- 62. Самарий
- 63. Европий
- 64. Гадолиний
- 65. Тербий
- 66. Диспрозий
- 67. Гольмий
- 68. Эрбий
- 69. Тулий
- 70. Иттербий
- 71. Лютеций
- 72. Гафний
- 73. Тантал
- 74. Вольфрам
- 75. Рений
- 76. Осмий
- 77. Иридий
- 78. Платина
- 79. Золото
- 80. Ртуть
- 81. Таллий
- 82. Свинец
- 83. Висмут
- 84. Полоний
- 85. Астат
- 86. Радон
- 87. Франций
- 88. Радий
- 89. Актиний
- 90. Торий
- 91. Протактиний
- 92. Уран
- 93. Нептуний
- 94. Плутоний
- 95. Америций
- 96. Кюрий
- 97. Берклий
- 98. Калифорний
- 99. Эйнштейний
- 100. Фермий
- 101. Менделеевий
- 102. Нобелий
- 103. Лоуренсий
- 104. Резерфордий
- 105. Дубний
- 106. Сиборгий
- 107. Борий
- 108. Хассий
- 109. Мейтнерий
- 110. Дармштадтий
- 111. Рентгений
- 112. Коперниций
- 113. Нихоний
- 114. Флеровий
- 115. Московий
- 116. Ливерморий
- 117. Теннессин
- 118. Оганесон
Таблица химических элементов Д.И. Менделеева




карта сайта
радон атомная масса степень окисления валентность плотность температура кипения плавления физические химические свойства структура теплопроводность электропроводность кристаллическая решетка
атом нарисовать строение число протонов в ядре строение электронных оболочек электронная формула конфигурация схема строения электронной оболочки заряд ядра состав масса орбита уровни модель радиус энергия электрона переход скорость спектр длина волны молекулярная масса объем атома
электронные формулы сколько атомов в молекуле радона радон
сколько электронов в атоме свойства металлические неметаллические термодинамические
Коэффициент востребованности 109
Радон описание химическиого элемента № 86
Радон открывали неоднократно, и в отличие от других подобных историй каждое новое открытие не опровергало, а лишь дополняло предыдущие. Дело в том, что никто из ученых не имел дела с элементом радоном — элементом в обычном для нас понимании этого слова. Одно из нынешних определений элемента — «совокупность атомов с общим числом протонов в ядре», т. е. разница может быть лишь в числе нейтронов. По существу элемент — совокупность изотопов.
РадонНо в первые годы нашего века еще не были открыты протон и нейтрон, не существовало самого понятия об изотопии.
Резерфорд и Оуэнс, Рамзай и Содди, Дорн, Дебьерн независимо друг от друга и практически одновременно (1900-1904 гг.) находили изотопы одного и того же элемента — элемента № 86. Все эти открытия были продолжением пионерских работ супругов Кюри в области радиоактивности. В каждом из этих исследований, как считали их авторы, был обнаружен свой, новый радиоактивный газ, новый элемент. Да и не могли они считать иначе: происхождение вновь открытых газов, их главная радиоактивная характеристика — период полураспада — были далеко не одинаковыми. Резерфордовскую эманацию (название происходит от латинского emanatio — «истечение») порождал торий. Дебьерновский актинон получался из актиния. Дорновский радон и рамзаевский нитон (от латинского nitens — «блестящий, светящийся») были дочерним продуктом радия…
Дорн открыл радон раньше Рамзая и Содди, тем не менее имена последних помещены в список первооткрывателей элемента № 86 заслуженно. Именно Рамзай первым исследовал свой нитон как химический элемент, выяснил характерные для него спектральные линии, определил атомную массу, объяснил химическую индифферентность и нашел место для этого элемента в периодической системе.
А хронологически первой из этих работ была работа Резерфорда и Оуэнса, проведенная в Канаде. Вот что рассказывал об этом в 1936 г. сам Резерфорд, ставший одним из корифеев новой физики. (Это фрагмент последнего публичного выступления Резерфорда, его доклада «Сорок лет развития физики».)
«… В 1898 г. я приехал в Мак-Гиллский университет в Монреале и там встретился с Р. Оуэнсом, новым профессором электротехники, который прибыл одновременно со мной. Оуэнс имел стипендию, которая обязывала его проводить некоторые физические исследования; он спросил, не могу ли я ему предложить тему, которую он мог бы исследовать для оправдания этой стипендии. Я предложил ему исследовать с помощью электроскопа торий, радиоактивность которого была тем временем открыта… Я помогал ему в проведении экспериментов, и мы обнаружили некоторые очень странные явления. Оказалось, что радиоактивное воздействие окиси тория может проходить сквозь дюжину листков бумаги, положенных поверх этой окиси, но задерживается тончайшей пластинкой слюды, как будто излучается что-то, способное диффундировать сквозь поры бумаги. Тот факт, что прибор был очень чувствителен к движению воздуха, поддерживал эту диффузионную гипотезу. Затем мы провели эксперименты, в которых воздух проходил над окисью тория, а потом попадал в ионизационную камеру. Эти опыты показали, что активность может переноситься воздухом. Однако когда поток воздуха прекращался, активность в ионизационной камере не сразу исчезала, а уменьшалась постепенно по экспоненциальному закону. Я назвал это газообразное вещество, которое может диффундировать сквозь бумагу, переноситься воздухом и в течение некоторого времени сохранять свою активность, исчезающую по характерному закону, «эманацией тория».
Я установил, что эта эманация обладает чрезвычайно своеобразным свойством делать радиоактивными тела, над которыми она проходит. Казалось, что это свойство скорее всего обусловлено осаждением некой материальной субстанции, а не какой-либо активностью, возникшей в самих телах под действием излучения, так как тогда количество осажденного вещества должно увеличиваться при приложении электрического поля. В те времена многие получали не повторяющиеся и странные результаты, помещая предметы вблизи радиоактивных веществ; по-видимому, все это могло объясняться наличием таких же эманаций, как обнаруженная нами у тория.
Прежде чем считать такое объяснение правильным, необходимо было выяснить истинную природу эманации. Это было очень трудно, так как доступное количество ее всегда было очень мало. С самого начала Содди и я предположили, что это, должно быть, инертный газ вроде гелия, неона или аргона, так как нам не удавалось заставить его соединиться с каким-либо химическим веществом…»
Дальше предположений, однако, Резерфорд не пошел — вероятно потому, что был не химиком, а физиком…
Справедливости ради теперь следовало бы предоставить слово химику. Сделаем это. Статья «Эманация», воспроизведенная здесь с сокращениями, написана в 1910 г. (можно сказать по горячим следам) выдающимся русским химиком профессором Львом Александровичем Чугаевым.
«Если какую-либо соль радия растворить в воде или нагреть в пустоте, то из нее освобождается радиоактивный газ, получивший название эманации. Этот газ обладает удивительнейшими свойствами. С одной стороны, он абсолютно инертен: все попытки ввести его в соединение с другими телами окончились неудачей… Но, с другой стороны, эманация принадлежит к самым активным и изменчивым телам, какие только можно себе представить. Она быстро разрушается, выбрасывая из себя альфа-частицы и теряя при этом свои радиоактивные свойства. Процесс этот, подобно другим превращениям радиоактивных веществ, совершается согласно рассмотренному нами выше закону мономолекулярных реакций. Константа у для эманации равна 0,000002, если в качестве единицы времени избрать секунду. Это значит, что в одну секунду из всего наличного количества эманации подвергается превращению 0,000002, или V500 000 часть.
Отсюда легко вычислить, что половина эманации разрушается в течение около четырех (точнее 3,86) дней.
Около -65°С при атмосферном давлении эманации сгущается в жидкость, малейшая капелька которой ярко флуоресцирует голубым или фиолетовым светом, который сравнивают с электрическим. При -71°С она застывает в твердую непрозрачную массу. Для этих опытов Резерфорд имел в своем распоряжении 0,14 г радия (давшие 0, 082 мм3 эманации), Рамзай — 0,39 г кристаллического бромистого радия, что соответствует 0,21 г металлического радия. При столь ничтожных количествах эманации ее приходилось собирать и наблюдать в тончайших капиллярных трубочках (диаметром 0,1-0,2 мм) под микроскопом. Определяя скорость, с которой эманация вытекает через тонкие отверстия, можно было найти (приблизительно, конечно) ее плотность, а отсюда вес молекулы, который (в наиболее надежных опытах) оказался близким к 220.
За последнее время (напоминаем, что статья написана в 1910 г. — Ред.) Рамзай и Грей пришли почти к тому же результату путем прямого взвешивания определенного объема эманации, заключенного в капиллярную кварцевую трубочку. Любопытен по своей тонкости экспериментальный прием, избранный ими для этой цели. Для взвешивания служили особые микровесы, целиком изготовленные из кварца. Чувствительность их достигала V500 000 мг, а наибольшее количество взвешиваемой эманации занимало объем не более 0,1 мм3. Самое взвешивание происходило без помощи разновесок. Взвешиваемое тело (кварцевый капилляр, содержащий эманацию) уравновешивалось одним и тем же полым кварцевым шариком, в котором было заключено некоторое количество воздуха. Вес этого шарика (кажущийся) менялся в зависимости от давления воздуха в приборе… Плотность эманации в среднем из ряда опытов была найдена равной 111,5, что соответствует молекулярному весу 223. Принимая во внимание, что эманация по своим свойствам должна быть причислена к индифферентным (в оригинале — «идеальным»; видимо, опечатка. — Ред.) газам нулевой группы, молекула которых всегда состоит из одного только атома, заключаем, что и атомный вес ее должен быть близок 223… И так как ныне уже нельзя сомневаться в ее элементарной природе, то Рамзай и предложил для нее особое название — нитон.
Процесс образования нитона из радия сопровождается выделением альфа-частиц, которые, как мы сейчас увидим, представляют из себя атомы гелия, заряженные положительным электричеством. Поэтому Резерфорд и Содди предположили, что первая фаза превращения радия выражается такой схемой: Ra = эманация + гелий (или Ra = Nt + Не), т. е. 226,4-4=222,4. На этом основании атомный вес нитона должен быть близок к 222,4.
Принимая во внимание трудность соответствующих экспериментальных определений, нельзя не признать совпадение прямо блестящим».
Что к этому следовало бы добавить?
Прежде всего, что за годы, прошедшие со дня открытия радона, его основные константы почти не уточнялись и не пересматривались. Это свидетельство высокого экспериментального мастерства тех, кто определил их впервые. Лишь температуру кипения (или перехода в жидкое состояние из газообразного) уточнили. В современных справочниках она указана вполне определенно — минус 62°С.
Еще надо добавить, что ушло в прошлое представление об абсолютной химической инертности радона, как, впрочем, и других тяжелых благородных газов. Еще до войны член-корреспондент Академии наук СССР Б.А. Никитин в ленинградском Радиевом институте получил и исследовал первые комплексные соединения радона — с водой, фенолом и некоторыми другими веществами. Уже из формул этих соединений: Rn-6H20, Rn -С6Н5ОН, Rn-CH3C6H5 — видно, что это так называемые соединения включения, что радон в них связан с молекулами воды или органического вещества лишь силами Ван-дер-Ваальса… Позже, в 60-х годах, были получены и истинные соединения радона. По сложившимся к этому времени теоретическим представлениям о галогенидах благородных газов, достаточной химической стойкостью должны обладать соединения радона RnF2, RnF4, RnCl4 и некоторые другие. Согласно тем же теоретическим представлениям, истинные химические соединения радона должны получаться легче, чем аналогичные соединения других благородных газов.
Фториды радона были получены сразу же после первых фторидов ксенона, однако точно идентифицировать их не удалось. Скорее всего, полученное малолетучее вещество представляет собой смесь фторидов радона. В отличие от довольно летучих фторидов ксенона, это вещество не возгоняется до температуры 250°С. Водород восстанавливает его при 500°С.
И наконец, заканчивая рассказ о химии радона, следует упомянуть об одном неудачном опыте, проделанном в начале века Резерфордом. Зная, что распад радия приводит к образованию гелия и радона, Резерфорд (не надеясь в общем-то на успех) попытался провести обратную реакцию: Rn + Не ^ Ra. Естественно, ничего из этого не получилось.
Что есть что
Радон, открытый Дорном, это самый долгоживущий изотоп элемента N° 86. Образуется при альфа-распаде радия-226. Массовое число этого изотопа — 222, период полураспада — 3,82 суток. Существует в природе как одно из промежуточных звеньев в цепи распада урана-238.
Эманация тория (торон), открытая Резерфордом и Оуэнсом, член другого естественного радиоактивного семейства — семейства тория. Это изотоп с массовым числом 220 и периодом полураспада 54,5 секунды.
Актинон, открытый Дебьерном, тоже член радиоактивного семейства тория. Это третий природный изотоп радона и из природных — самый короткоживугций. Его период полураспада меньше 4 секунд (точнее, 3,92 секунды), массовое число 219.
Нитон — то же самое, что радон
Всего сейчас известно 19 изотопов радона с массовыми числами 204 и от 206 до 224. Искусственным путем получено 16 изотопов. Нейтронодефицитные изотопы с массовыми числами до 212 получают в реакциях глубокого расщепления ядер урана и тория высокоэнергичными протонами. Эти изотопы нужны для получения и исследования искусственного элемента астата. Эффективный метод разделения нейтронодефицитных изотопов радона разработай в Объединенном институте ядерных исследований.
Долгое время «суммарным» названием элемента № 86 было слово «эманация». Собственно, до 1918 г. не было ни торона, ни актинона — были эманация тория и эманация актиния. Позже, однако, международные организации, ведающие химической номенклатурой, сделали общепринятым нынешнее название элемента № 86. С одной стороны, это можно объяснить стремлением к унификации: название «радон» более созвучно названиям прочих элементов, чем «эманация». А с другой стороны, все-таки именно радон оказался самой долгоживущей и самой полезной из всех эманаций…
Польза и вред радона
Радоновые ванныБесспорная польза и бесспорный вред. Сначала — о худшем: среди радиоактивных ядов радон — один из самых опасных. Не случайно допустимые, а тем более лечебные, терапевтические дозы радона чрезвычайно малы. Уже через час после введения в кровь кролику сравнительно небольшой дозы радона, 10 микрокюри, количество лейкоцитов в крови резко сокращается. Затем поражаются лимфатические узлы, селезенка, костный мозг…
Не столько сам радон задерживается в живом организме, сколько радиоактивные продукты его распада. Все исследователи, работавшие с твердым радоном, подчеркивают непрозрачность этого вещества. А причина непрозрачности одна: моментальное оседание твердых продуктов распада. Эти продукты «выдают» весь комплекс излучений: альфа-лучи — малопроникающие, но очень энергичные; бета-лучи; жесткое гамма-излучение…
Несмотря на это, радоновые ванны издавна занимают заметное место в арсенале курортологии и физиотерапии. Растворенный в воде радон (в ультрамикродозах) оказывает положительное воздействие на центральную нервную систему, на многие функции организма.
Медики полагают, что роль самого радона-222 здесь минимальна. Он же испускает лишь альфа-частицы, абсолютное большинство которых задерживается водой и на кожу не попадает. Зато активный налет продуктов распада радона продолжает действовать на организм и после прекращения процедуры. Радоновые ванны — эффективное средство лечения многих заболеваний — сердечно-сосудистых, кожных, а также нервной системы. Иногда радоновую воду прописывают и внутрь — для воздействия на органы пищеварения. Эффективны также радоновые грязи и вдыхание обогащенного радоном воздуха… Однако, как всякое сильнодействующее средство, радон требует постоянного врачебного контроля и очень точной дозировки. При некоторых заболеваниях радонотерапия абсолютно противопоказана.
Медицина использует как природные воды, содержащие радон, так и искусственно приготовленные. Радон получают из радия, и клинике вполне достаточно миллиграммов этого элемента, чтобы в течение долгого (по сути дела, неограниченно долгого) времени ежедневно готовить десятки радоновых ванн.
В природе радона очень мало — его можно отнести к числу наименее распространенных на нашей планете химических элементов. Содержание радона в атмосфере оценивается цифрой 7-1017% по весу. В земной коре его также очень мало — он же образуется преимущественно из сверхредкого радия. Тем не менее эти немногочисленные атомы очень заметны, с помощью специальных приборов разумеется.
Эти приборы называют эманометрами. Ими определяют, например, содержание радона в почвенном воздухе, и по этой характеристике судят о плотности и газопроницаемости горных пород. Засасывая воздух из буровых скважин с разных горизонтов, по содержанию радона определяют свойства горных пород на больших глубинах. По эманационным аномалиям геофизики судят о содержании радиоактивных руд в различных участках земной коры.
Эманирование — выделение радона твердыми телами, содержащими материнский элемент, зависит от температуры, влажности и структуры тела и меняется в очень широких пределах. Отсюда большие возможности эманационного метода исследования твердых веществ в промышленности и науке. Сравнительно недавно советскими учеными было установлено повышение концентрации радона и некоторых других элементов в подземных водах, находящихся близ эпицентра землетрясения. Это позволило создать метод прогноза землетрясений, который уже не раз оправдал себя на практике.
Излучение радона помогает исследовать состояние и дефекты различных материалов. В частности, радоновыми индикаторами пользуются для контроля противогазов на герметичность. Радон же помогает иногда следить за ходом технологических процессов в производстве таких несходных материалов, как сталь и стекло…
Применительно к радону эпитет «самый» можно повторять многократно: самый тяжелый, самый редкий, самый дорогой из всех существующих на Земле газов.
